��Ŀ����
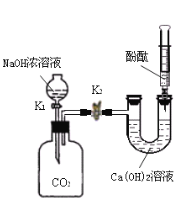
����Ŀ��������ʵ���ҷ�����һƿ���ڷ��õĹ���������Һ������Ϊ����Һ�����ʵ�����������С����Ҫ���²ⶨ�������Լ�ƿ�ı�ǩ������������ʵ�飺��������Һ34.0g�����ձ��У�Ȼ�������м���0.4g�������̣�ֱ�����ٷų�������ٳ����ձ��л������������������Ϊ33.6g��
��1�����ɵ����������Ϊ ��
��2�������ƿ����������Һ�����ʵ����������Ƕ��٣�
���𰸡�(1)0.8g;(2)5%
��������
�����������1�����ɵ����������Ϊ��34.0g+0.4g-33.6g=0.8g��
��2�������0.8g������Ҫ�������������Ϊx
2H2O2 ![]() 2H2O+ O2��
2H2O+ O2��
6832
x0.8g
68:32=x��0.8g
X=1.7g
�˹���������Һ�����ʵ���������Ϊ��
1.7g/34g��100%=5%��
�𣺸ù���������Һ�����ʵ���������Ϊ5%��

��ϰ��ϵ�д�
 53������ϵ�д�
53������ϵ�д�
�����Ŀ