题目内容
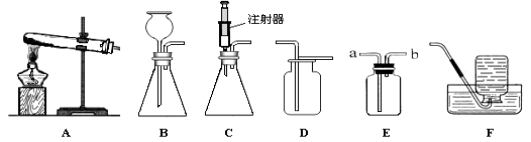
【题目】清理实验室时,发现如下三个内壁都有白色固体的细口瓶,曾经装过标签标示的溶液。现要清洗这些细口瓶,请你一起完成。

(1)三个瓶中的白色固体一定是纯净物的是 ;
(2)只用水不能清洗干净的细口瓶是 (填字母序号),形成这种固体的化学反应的方程式为 ;
(3)最后用稀盐酸和水将三个细口瓶洗净,洗后液体倒入一个干净的容器中,得到 澄清无色溶液,其中一定含有的溶质是 。
【答案】⑴C⑵B Ca(OH)2+CO2=CaCO3↓+H2O ⑶氯化钠和氯化钙
【解析】
试题分析:由两种或两种以上物质组成的物质叫混合物;由一种物质组成的物质叫纯净物;(1)氢氧化钠易和二氧化碳反应生成碳酸钠和水;氢氧化钙易和二氧化碳生成碳酸钙和水;氯化钠化学性质稳定,因此三个瓶中的白色固体一定是纯净物的是氯化钠;(2)氢氧化钠、碳酸钠、氯化钠易溶于水,可用水洗去,碳酸钙不溶于水,因此只用水不能清洗干净的细口瓶是B,形成这种固体的化学方程式是CO2+Ca(OH)2═CaCO3↓+H2O;(3)氢氧化钠和盐酸反应生成氯化钠和水,氢氧化钙和盐酸反应生成氯化钙和水,碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,因此最后溶液中一定有的溶质是氯化钠和氯化钙.

【题目】下表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
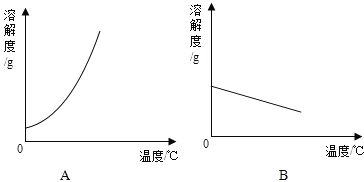
(1)依据上表数据,绘制Ca(OH)2和NaOH的溶解度曲线,如图所示能表示NaOH溶解度曲线的是 _________ (填A或B).
(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:①加入氢氧化钙,②升高温度,③降低温度,④加入水,⑤蒸发水后再恢复到原温度,⑥加入生石灰.
其中措施正确的是 _________.
A.②④⑥ B.③④ C.①③⑤⑥ D.①②⑤⑥
(3)20℃时,191g饱和NaOH溶液,蒸发10g水后,再降温到20℃,可析出NaOH晶体的质量为 _________ .
(4)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后得到的溶液(乙溶液),此时溶液中溶质的质量分数 乙 _________ 甲(填“>”、“<”或“=”).
(5)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是 _________ .
(6)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH _________ (填“偏大”、“偏小”或“不受影响”).
【题目】对下列事实或现象的解释错误的是
选项 | 事实或现象 | 解释 |
A | 八月桂花,十里飘香 | 分子总是在不断运动着 |
B | 水银温度计里的水银热胀冷缩 | 原子大小随温度改变而改变 |
C | 25m3石油气可加压装入0.024m3的钢瓶中 | 分子间是有间隔的 |
D | 一滴水中含千千万万个水分子 | 分子很小 |
A. A B. B C. C D. D