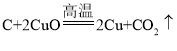题目内容
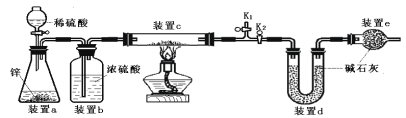
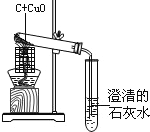
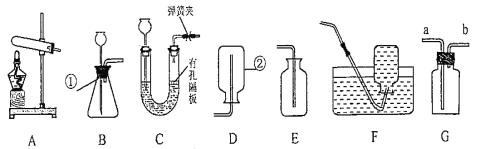
【题目】实验室制取气体所需装置如图所示。
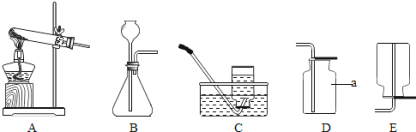
请回答以下问题:
(1)装置中标“a”的仪器名称是_____________。
(2)用高锰酸钾制取氧气时,所选用的发生装置是_____________(填字母,下同)。
(3)用大理石和稀盐酸制取二氧化碳时,所选用的发生装置是_____________。长颈漏斗在使用上的注意事项是:________________。
【答案】集气瓶 A、 B、 长颈漏斗底部应在液面以下,防止气体从长颈漏斗底部逸出
【解析】
(1)装置a为集气瓶,通常收集密度比空气大的气体,故填集气瓶;
(2)实验室用高锰酸钾制取氧气通常使用A装置,高锰酸钾为固体,需要加热,故填A;
(3)大理石为固体,稀盐酸是液体,不需要加热,实验室通常用长颈漏斗和锥形瓶进行发生反应装置,故填B;通过长颈漏斗加入稀盐酸时,必须保证长颈漏斗下端处于液面以下,保证产生的二氧化碳气体不会通过长颈漏斗逸出,故填长颈漏斗底部应在液面以下,防止气体从长颈漏斗底部逸出。

 天天练口算系列答案
天天练口算系列答案【题目】现代生活中,人们越来越注重微量元素的摄取。碘元素对人体健康有至关重要的作用。下表是某地市场销售的一种“加碘食盐”包装袋上的部分说明:
配料 | 氯化钠、碘酸钾KIO3 |
含碘量 | 20mg-30mg/kg |
保质期 | 18个月 |
食用方法 | 勿长时间炖炒 |
贮存方法 | 避光、避热、密封、防潮 |
请回答下列问题:(除第(1)小题外,其它题均需写出解题过程)
(1)由食用方法和贮存方法可推测碘酸钾的化学性质之一是______;
(2)计算碘酸钾KIO3中,钾元素、碘元素、氧元素的质量比______;
(3)计算碘酸钾KIO3中,碘元素的质量分数______;精确到0.01%
(4)计算1kg这样的食盐中,应加入______g碘酸钾,用最高含碘量计算;精确到0.01%
(5)若含碘量按最高量计算,若要摄入0.15mg的碘元素,则应补充该加碘食盐______g。