题目内容
【题目】甲、乙、丙三位同学在活动课上探究气体的制备。利用下图所示装置制取常见的气体,并对它们的有关性质进行研究,请根据题意回答下列问题。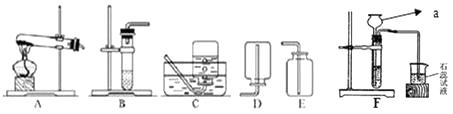
(1)实验仪器a的名称是
(2)甲同学用KMnO4固体制取O2 , 发生装置应选用上图中的 装置(填编号),该反应的化学方程式为 ;排水法,当O2收集满并取出集气瓶后,停止该实验的正确操作方法是 。
(3)乙同学用浓盐酸与大理石在F装置中反应,制取CO2并检验其有关性质,观察到烧杯中紫色石蕊试液变红,对这一现象解释不合理的是 (填序号)
a.产生的CO2直接使石蕊变红
b.产生的CO2与H2O反应生成H2CO3 , 使石蕊试液变红
c.挥发出的氯化氢溶于水,使石蕊试液变红
(4)丙同学在实验室氯化铵固体与碱石灰固体共热来制取氨气(NH3)。常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水。
①制取氨气反应的化学方程式2NH4Cl+ Ca(OH)2 ![]() CaCl2 + 2NH3↑+ 2X。 X的化学式为:。
CaCl2 + 2NH3↑+ 2X。 X的化学式为:。
②制取并收集NH3 , 应该从上图中选择的收集装置是 。
【答案】
(1)长颈漏斗
(2)A,2KMnO4 ![]() K2MnO4+MnO2+O2↑,先将导管移出水面,再熄灭酒精灯
K2MnO4+MnO2+O2↑,先将导管移出水面,再熄灭酒精灯
(3)a
(4)H2O,D
【解析】(1)实验仪器a的名称是长颈漏斗;(2)甲同学用KMnO4固体制取氧气需要加热,发生装置应选用图中的A,该反应的化学方程式为:2KMnO4 ![]() K2MnO4+MnO2+O2↑;当O2收集满并取出集气瓶后,防止水倒吸炸裂试管,停止该实验的正确操作方法是:先将导管移出水面,再熄灭酒精灯;(3)a.产生的二氧化碳不能直接使石蕊变红,错误; b.产生的CO2与H2O反应生成H2CO3,使石蕊试液变红,正确;c.挥发出的氯化氢溶于水,使石蕊试液变红,正确。故选a;(4)①由质量守恒定律和制取氨气反应的化学方程式2NH4Cl + Ca(OH)2
K2MnO4+MnO2+O2↑;当O2收集满并取出集气瓶后,防止水倒吸炸裂试管,停止该实验的正确操作方法是:先将导管移出水面,再熄灭酒精灯;(3)a.产生的二氧化碳不能直接使石蕊变红,错误; b.产生的CO2与H2O反应生成H2CO3,使石蕊试液变红,正确;c.挥发出的氯化氢溶于水,使石蕊试液变红,正确。故选a;(4)①由质量守恒定律和制取氨气反应的化学方程式2NH4Cl + Ca(OH)2 ![]() CaCl2 + 2NH3↑+ 2X,据反应前后原子的种类和数目不变可知X的化学式为:H2O;
CaCl2 + 2NH3↑+ 2X,据反应前后原子的种类和数目不变可知X的化学式为:H2O;
②氨气极易溶于水,不能用排水法收集,密度比空气小,可以用向下排空气法收集,即用D装置收集。
故答案为:长颈漏斗;A;2KMnO4 K2MnO4+MnO2+O2↑;先将导管移出水面,再熄灭酒精灯;a;H2O;D。
本题主要考察气体制备装置的选择,在气体制备时,发生装置的选择要根据药品状态和反应所需要的条件选择发生装置,收集装置的选择主要考虑气体的密度和溶解性以及能否于水发生反应。在化学反应中,反应前后原子种类和数目保持不变。

【题目】下表提供了硝酸钾固体在不同温度时的溶解度
温度/℃ | 0 | 20 | 40 | 60 | 80 |
溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
现有60℃时的硝酸钾饱和溶液420g,若降温至0℃,析出硝酸钾晶体的质量为( )
A. 206.7gB. 188.4gC. 193.4gD. 156.8g