题目内容
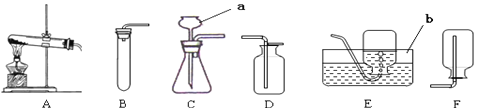
【题目】小菁和几位同学在实验室用下列装置制取气体。
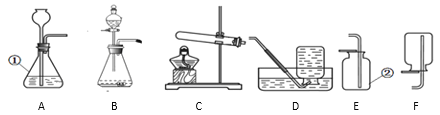
(1)图中标有①、②的仪器名称:①_________; ②__________。
(2)A装置中长颈漏斗下端要插入液面以下,其目的是:____________________。
(3)C装置中试管口略向下倾斜的目的是__________________________ 。
(4)小菁若用氯酸钾制取较干燥的氧气,应选用的发生装置为______ (填字母),收集装置为______,用该收集方法收集氧气后验满氧气的方法是____________,该反应化学方程式为_______________,反应类型为_________________反应。
(5)氯酸钾制氧气反应完全发生后要将试管中的固体剩余物按照以下流程进行分离。
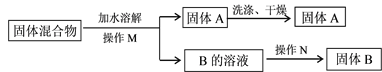
操作N的名称是______,固体A是___________,固体A作用是_____________。
(6)小明同学选用双氧水制氧气,要制取0.03mol氧气,理论上至少需要过氧化氢的物质的量为________。(根据化学方程式列式计算,写出计算过程)
(7)催化剂探究
学习了MnO2对过氧化氢分解有催化作用的知识后,小菁同学查阅资料后发现氧化铁也可做过氧化氢分解的催化剂,为了比较相同条件下氧化铁和二氧化锰对该反应的催化效果哪个好,于是他和自己的小组成员一起进行了以下探究。
【实验目的】________________________________________。
【实验方案】常温下,在盛有相同质量的二氧化锰和氧化铁的两个容器中,分别放入相同体积的3%的过氧化氢溶液,测量各生成1瓶(相同体积)氧气,所需的时间。
【实验仪器】量筒、胶头滴管、药匙
【实验数据】
实验编号 | 双氧水的浓度 | 催化剂种类(a g) | 时间(min) |
1 | 3% | 氧化铁 | 16.0 |
2 | 3% | 二氧化锰 | 2.0 |
【结论】该实验的结论是________________________________________。
【答案】 锥形瓶 集气瓶 防止气体从其上端逸出(液封) 防止水(冷凝的水)倒流使试管炸裂 C E 将带火星的木条放在集气瓶口,若复燃,则满 2KClO3![]() 2KCl+3O2↑ 分解 蒸发 MnO2 加快反应速度(催化作用) 0.06 比较相同条件下氧化铁和二氧化锰对过氧化氢分解的催化效果(合理即给分) 相同条件下二氧化锰比氧化铁对过氧化氢分解的催化效果好(合理即给分)
2KCl+3O2↑ 分解 蒸发 MnO2 加快反应速度(催化作用) 0.06 比较相同条件下氧化铁和二氧化锰对过氧化氢分解的催化效果(合理即给分) 相同条件下二氧化锰比氧化铁对过氧化氢分解的催化效果好(合理即给分)
【解析】(1)由图可知①是锥形瓶,②是集气瓶;(2)A装置中为了避免气体从其上端逸出,故长颈漏斗下端要插入液面以下;(3)加热固体时试管口要略向下倾斜,目的是防止水(冷凝的水)倒流使试管炸裂;(4)根据反应物的状态和反应条件选择发生装置,用加热氯酸钾的方法制取氧气属固固加热型,故发生装置选C;根据题意,要制取一瓶比较干燥的氧气,结合氧气的密度比空气大可知,可用向上排空气法收集E,用向上排空气法收集氧气验满的方法是将带火星的木条放在集气瓶口,若复燃,则表示收集满了;氯酸钾在加热和二氧化锰的催化作用下分解生成氧气的同时还生成了氯化钾,反应的化学方程式表示为2KClO3 ![]() 2KCl+3O2↑,该反应的反应物是一种,生成物是两种,属分解反应;(5)氯酸钾制氧气反应完全发生后试管中的固体剩余物是氯化钾和二氧化锰,氯化钾易溶于水,二氧化锰难溶于水,故可将固体溶解后过滤,可得到固体二氧化锰和滤液氯化钾溶液,氯化钾溶液经蒸发后可得到固体氯化钾,故操作N是蒸发,固体A是二氧化锰,二氧化锰是氯酸钾分解的催化剂,起催化作用;(6)利用化学方程式,根据反应的物质的量之比即可计算出需要的过氧化氢的物质的量。设需要的过氧化氢的物质的量为x,
2KCl+3O2↑,该反应的反应物是一种,生成物是两种,属分解反应;(5)氯酸钾制氧气反应完全发生后试管中的固体剩余物是氯化钾和二氧化锰,氯化钾易溶于水,二氧化锰难溶于水,故可将固体溶解后过滤,可得到固体二氧化锰和滤液氯化钾溶液,氯化钾溶液经蒸发后可得到固体氯化钾,故操作N是蒸发,固体A是二氧化锰,二氧化锰是氯酸钾分解的催化剂,起催化作用;(6)利用化学方程式,根据反应的物质的量之比即可计算出需要的过氧化氢的物质的量。设需要的过氧化氢的物质的量为x,
2H2O2 MnO2 2H2O+O2↑
2 1
X 0.03mol
![]() x=0.06mol
x=0.06mol
(7)由题意可知,该实验的目的是比较相同条件下氧化铁和二氧化锰对过氧化氢分解的催化效果;由表格数据可知收集等体积的氧气,当催化剂是二氧化锰时需要的时间较短,即相同条件下二氧化锰比氧化铁对过氧化氢分解的催化效果好。

【题目】鉴别物质的方法或试剂正确的是
选项 | 待鉴别的物质 | 所选试剂或方法 |
A | 氮气和二氧化碳 | 燃烧的木条 |
B | 二氧化锰和氧化铜 | 观察颜色 |
C | 水和双氧水 | 二氧化锰 |
D | 氢氧化钠溶液和碳酸钠溶液 | 无色酚酞试液 |
A.AB.BC.CD.D