题目内容
(2009?南京一模)钢铁工业是一个国家的支柱产业之一.如图1是工业炼铁的基本生产流程示意图.请回答下列问题: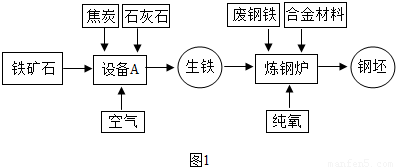
(1)写出图1中设备A 的名称:______;
(2)写出以赤铁矿为原料在高温下制取铁的化学方程式______ 2Fe+3CO2
【答案】分析:(1)工业炼铁又称为高炉炼铁,因为工业炼铁使用的设备为高炉;
(2)赤铁矿石中的氧化铁在高温下与一氧化碳反应,生成铁和二氧化碳;
(3)碳酸钙高温锻烧可分解生成氧化钙和二氧化碳;
(4)根据反应记录数据,完全反应放出氢气质量=159.0g-158.7g=0.3g,加入稀硫酸的质量=159.0g-44.1g-9.0g=105.9g;结合反应的化学方程式,由生成氢气的质量计算生铁中铁的质量、反应生成硫酸亚铁的质量等,完成分析和计算.
解答:解:(1)工业炼铁所使用的设备为高炉,炼铁过程是在高炉内完成的;
故答案为:高炉;
(2)赤铁矿中的氧化铁在高温下与一氧化碳发生氧化还原反应,生成单质铁和气体二氧化碳;
故答案为:3CO+Fe2O3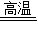 2Fe+3CO2;
2Fe+3CO2;
(3)石灰石的主要成分碳酸钙在高温锻烧时分解生成氧化钙和二氧化碳;
故答案为:CaCO3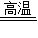 CaO十CO2↑;
CaO十CO2↑;
(4)①由于生铁样品中的杂质不溶于水且不与酸发生反应,因此反应停止后样品的质量不为0;所以图A所示的分析错误;
随着生铁不断与稀硫酸反应,放出氢气质量逐渐增大,至完全反应,放出氢气的质量=159.0g-158.7g=0.3g;所以图B的分析正确;
加入稀硫酸的质量=159.0g-44.1g-9.0g=105.9g,反应使溶液的质量逐渐增大,直到反应停止溶液质量不再改变;所以图C的分析错误;
故答案为:B;
②③设反应的铁的质量为x,生成的硫酸亚铁的质量为y
Fe+H2SO4═FeSO4+H2↑
56 152 2
x y 0.3g
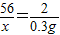 解得 x=8.4g
解得 x=8.4g
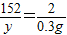 解得 y=22.8g
解得 y=22.8g
铁的质量分数=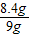 ×100%=93.3%
×100%=93.3%
硫酸亚铁的溶质质量分数=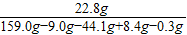 ×100%=20%
×100%=20%
答:样品中铁的质量分数为93.3%,硫酸亚铁的溶质质量分数为20%.
点评:根据质量守恒定律,反应后所得溶液的质量=所加稀盐酸的质量+参加反应铁的质量-放出氢气的质量.
(2)赤铁矿石中的氧化铁在高温下与一氧化碳反应,生成铁和二氧化碳;
(3)碳酸钙高温锻烧可分解生成氧化钙和二氧化碳;
(4)根据反应记录数据,完全反应放出氢气质量=159.0g-158.7g=0.3g,加入稀硫酸的质量=159.0g-44.1g-9.0g=105.9g;结合反应的化学方程式,由生成氢气的质量计算生铁中铁的质量、反应生成硫酸亚铁的质量等,完成分析和计算.
解答:解:(1)工业炼铁所使用的设备为高炉,炼铁过程是在高炉内完成的;
故答案为:高炉;
(2)赤铁矿中的氧化铁在高温下与一氧化碳发生氧化还原反应,生成单质铁和气体二氧化碳;
故答案为:3CO+Fe2O3
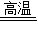 2Fe+3CO2;
2Fe+3CO2;(3)石灰石的主要成分碳酸钙在高温锻烧时分解生成氧化钙和二氧化碳;
故答案为:CaCO3
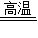 CaO十CO2↑;
CaO十CO2↑;(4)①由于生铁样品中的杂质不溶于水且不与酸发生反应,因此反应停止后样品的质量不为0;所以图A所示的分析错误;
随着生铁不断与稀硫酸反应,放出氢气质量逐渐增大,至完全反应,放出氢气的质量=159.0g-158.7g=0.3g;所以图B的分析正确;
加入稀硫酸的质量=159.0g-44.1g-9.0g=105.9g,反应使溶液的质量逐渐增大,直到反应停止溶液质量不再改变;所以图C的分析错误;
故答案为:B;
②③设反应的铁的质量为x,生成的硫酸亚铁的质量为y
Fe+H2SO4═FeSO4+H2↑
56 152 2
x y 0.3g
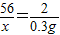 解得 x=8.4g
解得 x=8.4g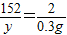 解得 y=22.8g
解得 y=22.8g铁的质量分数=
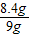 ×100%=93.3%
×100%=93.3%硫酸亚铁的溶质质量分数=
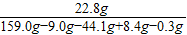 ×100%=20%
×100%=20%答:样品中铁的质量分数为93.3%,硫酸亚铁的溶质质量分数为20%.
点评:根据质量守恒定律,反应后所得溶液的质量=所加稀盐酸的质量+参加反应铁的质量-放出氢气的质量.

练习册系列答案
相关题目
(2009?南京一模)下列各图象能正确反映所对应的实验事实的是( )


| 选项 | 实验事实 |
| A | 充分加热等质量的氯酸钾制氧气 |
| B | 往稀硫酸中加入氯化钡溶液至过量 |
| C | 滴加稀盐酸恰好中和pH=13的氢氧化钾溶液 |
| D | t℃向某接近饱和的硫酸钠溶液中缓慢加入硫酸钠粉末(a%为该溶液溶质质量分数) |
