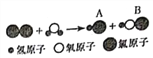
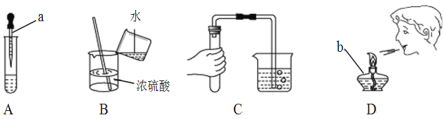
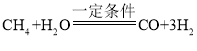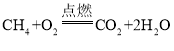题目内容
【题目】) 钢铁是使用最多的金属材料。
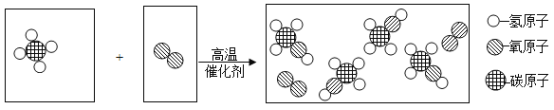
⑴早在春秋战国时期,我国就开始生产和使用铁器。写出以赤铁矿(主要成分Fe2O3)为原料炼铁的化学方程式__________________________。
⑵利用新技术能将不锈钢加工成柔软的金属丝,用它和棉纤维一起编织成性能优良的劳保防护服,这是利用了不锈钢的________(填序号)。
A 耐腐蚀性 B 延展性 C 导热性 D 导电性
⑶市场上有一种含铁粉的麦片,食用后在胃酸作用下将铁粉转化为人体可吸收的铁元素,反应的化学方程式为________________________。这种麦片必须真空保存,原因是____________________________________________________。
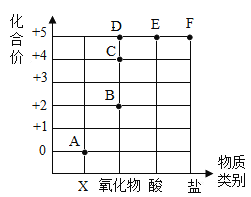
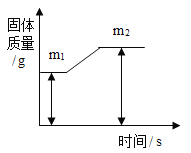
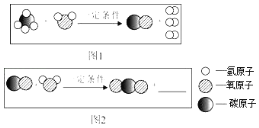
(4)为探究铁和锌两种金属与酸反应的状况,将等质量的两种金属分别与等质量的溶质质量分数相同的稀硫酸反应,产生氢气的质量与反应时间的函数关系如图所示。下列相关判断中,正确的是_______
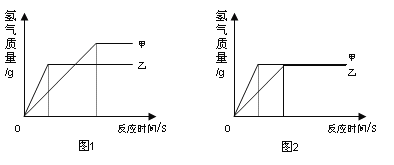
A 甲是铁,乙是锌
B 甲是锌,乙是铁
C 图1表示稀硫酸足量,图2表示稀硫酸不足量
D 图1表示金属一定有剩余,图2表示金属一定没有剩余
【答案】3CO+Fe2O3![]() 2Fe+3CO2 A、B Fe+2HCl=FeCl2+H2↑ 与空气中的氧气和水接触生锈而变质 A 、C
2Fe+3CO2 A、B Fe+2HCl=FeCl2+H2↑ 与空气中的氧气和水接触生锈而变质 A 、C
【解析】
(1)以赤铁矿(主要成分Fe2O3)为原料炼铁发生的反应是氧化铁与一氧化碳在高温条件下反应生成铁和二氧化碳,反应的化学方程式为3CO+Fe2O3![]() 2Fe+3CO2;
2Fe+3CO2;
(2)将不锈钢加工成柔软的金属丝,这是利用了不锈钢的耐腐蚀性和延展性,故选A、B;
(3)含铁粉的麦片在胃酸作用下将铁粉转化为人体可吸收的铁元素,反应的化学方程式为Fe+2HCl=FeCl2+H2↑。这种麦片必须真空保存,原因是其中的铁会与空气中的氧气和水接触生锈而变质;
(4)A、锌比铁活泼,和稀硫酸反应速率较快,反应需要时间短,最终铁和稀硫酸反应生成的氢气多,因此甲是铁,乙是锌,故A正确;
B、根据A选项分析可知,甲是铁,乙是锌,故B错误;
C、图1中金属锌与稀硫酸充分反应后,稀硫酸可能还有剩余(稀硫酸过量时),也可能没有剩余(锌和稀硫酸恰好完全反应),图1表示稀硫酸足量;图2中产生的氢气质量相等,表示稀硫酸不足量,金属足量,故C正确;
D、图2中最终生成氢气质量相等,说明稀硫酸完全反应,铁一定有剩余,故D错误。故选AC。

【题目】热水瓶胆水垢的主要成分是Mg(OH)2和CaCO3,可用适量盐酸清洗除去.小红为测定水垢中碳酸钙的质量分数,进行了如下实验:取200g水垢,往其中逐滴加入足量的稀盐酸,将产生的气体缓缓通入足量氢氧化钠溶液中,同时测量8min内氢氧化钠溶液质量的变化值.所得结果如下表所示(忽略稀盐酸的挥发).
时间(min) | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
氢氧化钠溶液增加的质量(g) | 0 | 13 | 24 | 32 | 31 | 41 | 43 | 44 | 44 |
(1)表中有一个时间测量的“氢氧化钠溶液增加的质量”数据是错误的,此时间是第__min;
(2)200g水垢溶于足量稀盐酸中,产生CO2的最大质量为______g;
(3)计算水垢中碳酸钙的质量分数.________
(4)请在如图坐标图中用正确的数据描绘出氢氧化钠溶液增加的质量与时间的变化关系图.__________

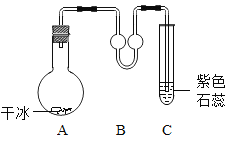
【题目】酒精灯是实验室中常用加热仪器,某兴趣小组同学对酒精灯进行如下探究。
(Ⅰ)定性研究甲同学取一根火柴梗,拿住一端迅速平放入酒精灯火焰中,1~2s后取出,观察到位于焰心的部分没有明显变化,说明焰心温度最低。
(1)写出碳完全燃烧的文字表达式(或符号表达式)__________。
(Ⅱ)定量研究
乙同学用注射器抽取灯芯和焰心交界处气体,利用氧气传感器测量氧气的体积分数(见下表),丙同学利用高温传感器测定酒精灯灯芯和焰心交界处温度(见下表)。
测量次数 | 第一次 | 第二次 | 第三次 |
灯芯和焰心交界处 氧气体积分数 | 5.93% | 5.29% | 6.53% |
灯芯和焰心交界处温度/℃ | 236 | 243 | 240 |
(2)乙、丙同学多次进行测量的目的是_____。
(3)火柴梗燃烧需要氧气的最低含量是14.0%,着火点是270℃,结合上表谈谈你对“火柴梗在焰心处没有明显变化”的认识_____。
(4)如果考虑抽气时空气的影响,则乙同学测出的氧气浓度比焰心的实际氧气浓度_____。(填“高”或“低”):另外乙同学所测氧气的体积分数差异的原因可能是①_____;②_____。