题目内容
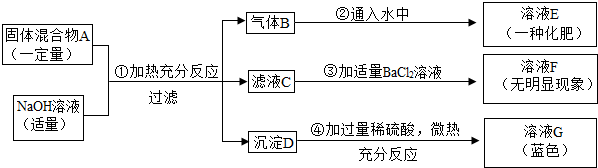
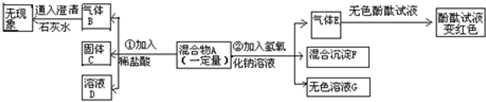
现欲探究一固体混合物A的成分,已知其中可能含有Fe、Na2CO3、CuO、(NH4)2SO4四种物质中的两种或多种.按如图所示进行实验,出现的现象如图中所述(设过程中所有可能发生的反应都恰好完全反应).
(1)气体E的化学式为
(2)混合物A中一定存在的物质有
(3)溶液D为
(4)溶液G中存在的酸根离子为
(5)写出实验过程①中生成气体B的化学方程式

(1)气体E的化学式为
NH3
NH3
.(2)混合物A中一定存在的物质有
Fe、CuO、(NH4)2SO4
Fe、CuO、(NH4)2SO4
.(3)溶液D为
浅绿
浅绿
色.(4)溶液G中存在的酸根离子为
硫酸根离子
硫酸根离子
.(5)写出实验过程①中生成气体B的化学方程式
Fe+2HCl═FeCl2+H2↑
Fe+2HCl═FeCl2+H2↑
.分析:将混合物加入稀盐酸中产生的气体不能使澄清石灰水变浑浊,说明该气体为氢气,即混合物中含有铁,而没有碳酸钠;将混合物加入到氢氧化钠溶液中,产生了气体使无色的酚酞试液变红,说明产生的气体为氨气,进而可以判断混合物中含有硫酸铵;同时得到了混合沉淀F,结合铁和氧化铜不能溶于碱液中,所以可以判断一定含有的物质为铁、氧化铜和硫酸铵,可以据此来分析变完成各题的解答.
解答:解:(1)根据分析知道,将混合物加入到氢氧化钠溶液中,产生了气体使无色的酚酞试液变红,说明产生的气体为氨气;
(2)根据分析可以知道,将混合物加入稀盐酸中产生的气体不能使澄清石灰水变浑浊,说明该气体为氢气,即混合物中含有铁,而没有碳酸钠;将混合物加入到氢氧化钠溶液中,产生了气体使无色的酚酞试液变红,说明产生的气体为氨气,进而可以判断混合物中含有硫酸铵;同时得到了混合沉淀F,结合铁和氧化铜不能溶于碱液中,所以可以判断一定含有的物质为铁、氧化铜和硫酸铵;
(3)根据(1)的解答可以知道:因为混合物中有铁的存在,所以铁要和氯化铜反应,而生成铜和氯化亚铁,所以可以判断D为氯化亚铁溶液,其溶液为浅绿色;
(4)根据(2)的解答可以知道溶液G为硫酸钠溶液,所以可以判断该溶液中含有的阴离子为硫酸根离子;
(5)根据(1)的解答可以知道生成的B为氢气,该反应为铁和硫酸的反应,所以可以判断该反应的化学方程式为:Fe+2HCl═FeCl2+H2↑.
故答案为:(1)NH3;
(2)Fe、CuO、(NH4)2SO4;
(3)浅绿;
(4)硫酸根离子;
(5)Fe+2HCl═FeCl2+H2↑.
(2)根据分析可以知道,将混合物加入稀盐酸中产生的气体不能使澄清石灰水变浑浊,说明该气体为氢气,即混合物中含有铁,而没有碳酸钠;将混合物加入到氢氧化钠溶液中,产生了气体使无色的酚酞试液变红,说明产生的气体为氨气,进而可以判断混合物中含有硫酸铵;同时得到了混合沉淀F,结合铁和氧化铜不能溶于碱液中,所以可以判断一定含有的物质为铁、氧化铜和硫酸铵;
(3)根据(1)的解答可以知道:因为混合物中有铁的存在,所以铁要和氯化铜反应,而生成铜和氯化亚铁,所以可以判断D为氯化亚铁溶液,其溶液为浅绿色;
(4)根据(2)的解答可以知道溶液G为硫酸钠溶液,所以可以判断该溶液中含有的阴离子为硫酸根离子;
(5)根据(1)的解答可以知道生成的B为氢气,该反应为铁和硫酸的反应,所以可以判断该反应的化学方程式为:Fe+2HCl═FeCl2+H2↑.
故答案为:(1)NH3;
(2)Fe、CuO、(NH4)2SO4;
(3)浅绿;
(4)硫酸根离子;
(5)Fe+2HCl═FeCl2+H2↑.
点评:此题为框图式物质推断题,完成此类题目,关键是找准解题突破口,直接得出结论,然后利用顺向或逆向或两边向中间推,逐一导出其他结论.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目