题目内容
【题目】取CaCl2和CaCO3的混合物12.5g于烧杯中,向其中滴加一定溶质质量分数的稀盐酸,请加稀盐酸的质量与产生气体质量的关系如图所示.求: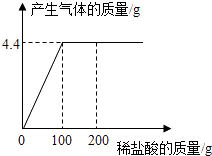
(1)混合物CaCO3中的质量为;
(2)稀盐酸中的溶质质量分数为;
(3)恰好完全反应时,所得不饱和溶液中溶质的质量分数?(写出计算过程,计算结果精确到0.1%)
【答案】
(1)10g
(2)7.3%
(3)
解:盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,由图可知:二氧化碳的质量为4.4g
设碳酸钙的质量为x,稀盐酸中的溶质质量为z,生成氯化钙的质量为y.
CaCO3+ | 2HCl= | CaCl2+H2O+ | CO2↑ |
100 | 73 | 111 | 44 |
x | y | z | 4.4g |
![]()
x=10g
z=7.3g
y=11.1g
恰好完全反应时,所得不饱和溶液中溶质的质量分数= ![]() 100%≈12.6%
100%≈12.6%
答:恰好完全反应时,所得不饱和溶液中溶质的质量分数为12.6%
【解析】解:盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,由图可知:二氧化碳的质量为4.4g
设碳酸钙的质量为x,稀盐酸中的溶质质量为z,生成氯化钙的质量为y.
CaCO3+ | 2HCl= | CaCl2+H2O+ | CO2↑ |
100 | 73 | 111 | 44 |
x | y | z | 4.4g |
![]()
x=10g
z=7.3g
y=11.1g(1)混合物CaCO3中的质量为10g;(2)稀盐酸中的溶质质量分数为 ![]() 100%=7.3%;
100%=7.3%;
答案:(1)10g;(2)7.3%;(3)所得不饱和溶液中溶质的质量分数12.6%.
根据盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,利用二氧化碳的质量,然后利用化学方程式计算出反应的碳酸钙的质量、稀盐酸中的溶质质量以及生成氯化钙的质量.然后利用氯化钙的质量,计算出反应后所得溶液中溶质的质量分数即可.

 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案【题目】化学兴趣小组的同学发现实验台上一瓶标签破损的无色溶液(标签如图).他们提出可能是Na2SO4、NaHCO3、Na2CO3溶液中的一种,于是决定对这瓶溶液进行实验探究.查阅资料:三种物质溶液在常温下的PH如下表
溶液 | Na2SO4 | NaHCO3 | Na2CO3 |
pH | pH=7 | pH>7 | pH>7 |
(1)小新同学认为该溶液 ![]() 的是 , 理由是 .
的是 , 理由是 .
(2)标签破损的原因 .
(3)为确定其成分,小新同学设计如下方案进行探究
实验步骤 | 现象 | 结论 |
取该溶液少许于试管中,滴加过量的BaCl2溶液,振荡. | ① | 则该溶液是Na2CO3溶液 |
过滤,向滤渣滴加稀盐酸. | ② |
(4)小芳认为可以设计更简单的实验方案,该方案是:(写出实验步骤、现象及结论). 