题目内容
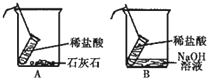 小刚和小洁以“化学反应中,反应物和生成物的质量关系”为课题进行科学探究,请填写以下探究过程中的空格:
小刚和小洁以“化学反应中,反应物和生成物的质量关系”为课题进行科学探究,请填写以下探究过程中的空格:(1)提出假设:化学反应中,反应物的总质量与生成物的总质量
相等
相等
.(2)确定研究方法:分析推理,查阅资料,实验探究.
(3)设计并进行实验:小刚设计的实验装置和选用药品如图A所示,小洁的如图B所示,他们在反应前后都进行了规范的操作,准确的称量和细致的观察.实验B中反应的化学方程式是
NaOH+HCl═NaCl+H2O
NaOH+HCl═NaCl+H2O
;实验A、B中的两个反应都属于复分解
复分解
反应.(4)实验结论:通过实验,小刚认为:在化学反应中,生成物的总质量与反应物的总质量不相等;小洁认为:在化学反应中生成物的总质量与反应物的总质量相等.你认为结论正确的是
小洁
小洁
,请你谈谈导致另一种结论错误的原因:小刚在操作过程中反应生成的CO2气体逸出锥形瓶,所以剩余的生成物的质量比反应物的总质量减少了.
小刚在操作过程中反应生成的CO2气体逸出锥形瓶,所以剩余的生成物的质量比反应物的总质量减少了.
.(5)结论分析:请从原子的角度,简要分析你认为正确的结论:
在化学反应中,反应前后原子的种类没有改变,原子的数目没有增减,原子的质量没有变化,所以,在化学反应中,反应物的质量总和与生成物的质量总和必然相等.
在化学反应中,反应前后原子的种类没有改变,原子的数目没有增减,原子的质量没有变化,所以,在化学反应中,反应物的质量总和与生成物的质量总和必然相等.
.(6)查阅资料:小刚和小洁通过查阅资料了解到:法国伟大的科学家拉瓦锡,早在18世纪就围绕这个问题,进行了准确,缜密的研究,并作出了科学结论.
(7)结论应用:环保部门常用I2O5测定空气受CO污染的程度,发生反应的化学方程式:I2O5+5CO═I2+5X.根据生成X的多少,可以判断CO的含量,X的化学式是
CO2
CO2
.分析:盐酸和石灰石反应生成了氯化钙、水、二氧化碳,生成的二氧化碳气体跑出质量减少,天平不平衡,所以不能用来验证质量守恒;稀盐酸与氢氧化钠反应生成氯化钠和水,没有物质跑出,质量不变,能验证质量守恒.根据化学反应的实质来解释质量守恒定律,利用质量守恒定律推断物质化学式.
解答:解:(1)化学反应都遵守质量守恒定律,所以,提出假设:化学反应中,反应物的总质量与生成物的总质量相等;
(3)在A中碳酸钙与盐酸反应,反应的方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑,在B中氢氧化钠与盐酸反应的方程式:NaOH+HCl═NaCl+H2O;都是由两种化合物相互交换了成分生成了两种新的化合物,属于复分解反应;
(4)由上述反应及装置可知可.小洁用的是氢氧化钠与盐酸的反应,生成了氯化钠和水,没有气体跑出,反应前后质量相等.所以小洁结论正确;由于小刚在操作过程中反应生成的CO2气体逸出锥形瓶,所以剩余的生成物的质量比反应物的总质量减少了,天平发生了偏向,不能用来验证质量守恒定律;
(5)化学反应的实质是分子分成原子,原子再重新组合成新的分子,所以反应前后原子的种类没有改变,原子的数目没有增减,原子的质量没有变化,所以,在化学反应中,反应物的质量总和与生成物的质量总和必然相等;
(7)在方程式的左边有碘、氧、碳的原子的个数分别是2、10、5,在最右边有碘的原子的个数是2,由于反应前后原子的个数不变,生成物中还少10个氧原子,5个碳原子,又因为X前面系数是5,所以X的化学式是CO2.
故答案为:(1)相等;(3)NaOH+HCl═NaCl+H2O,复分解;(4)小洁,小刚在操作过程中反应生成的CO2气体逸出锥形瓶,所以剩余的生成物的质量比反应物的总质量减少了.(5)在化学反应中,反应前后原子的种类没有改变,原子的数目没有增减,原子的质量没有变化,所以,在化学反应中,反应物的质量总和与生成物的质量总和必然相等;(7)CO2.
(3)在A中碳酸钙与盐酸反应,反应的方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑,在B中氢氧化钠与盐酸反应的方程式:NaOH+HCl═NaCl+H2O;都是由两种化合物相互交换了成分生成了两种新的化合物,属于复分解反应;
(4)由上述反应及装置可知可.小洁用的是氢氧化钠与盐酸的反应,生成了氯化钠和水,没有气体跑出,反应前后质量相等.所以小洁结论正确;由于小刚在操作过程中反应生成的CO2气体逸出锥形瓶,所以剩余的生成物的质量比反应物的总质量减少了,天平发生了偏向,不能用来验证质量守恒定律;
(5)化学反应的实质是分子分成原子,原子再重新组合成新的分子,所以反应前后原子的种类没有改变,原子的数目没有增减,原子的质量没有变化,所以,在化学反应中,反应物的质量总和与生成物的质量总和必然相等;
(7)在方程式的左边有碘、氧、碳的原子的个数分别是2、10、5,在最右边有碘的原子的个数是2,由于反应前后原子的个数不变,生成物中还少10个氧原子,5个碳原子,又因为X前面系数是5,所以X的化学式是CO2.
故答案为:(1)相等;(3)NaOH+HCl═NaCl+H2O,复分解;(4)小洁,小刚在操作过程中反应生成的CO2气体逸出锥形瓶,所以剩余的生成物的质量比反应物的总质量减少了.(5)在化学反应中,反应前后原子的种类没有改变,原子的数目没有增减,原子的质量没有变化,所以,在化学反应中,反应物的质量总和与生成物的质量总和必然相等;(7)CO2.
点评:在设计验证质量守恒的实验时要考虑实验在密闭容器中进行,组装装置时注意实验的准确性和安全性.

练习册系列答案
相关题目
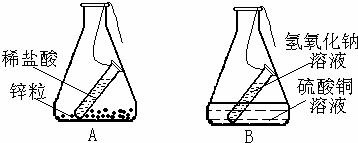

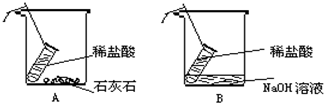 小刚和小洁以“化学反应中,反应物和生成物的质量关系”为课题进行科学探究,请填写以下探究过程中的空格:(提示:稀盐酸与石灰石反应生成二氧化碳和水、氯化钙;与氢氧化钠生成水和氯化钠)
小刚和小洁以“化学反应中,反应物和生成物的质量关系”为课题进行科学探究,请填写以下探究过程中的空格:(提示:稀盐酸与石灰石反应生成二氧化碳和水、氯化钙;与氢氧化钠生成水和氯化钠)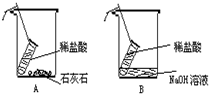 小刚和小洁以“化学反应中,反应物和生成物的质量关系”为课题进行科学探究,请填写以下探究过程中的空格:(提示:稀盐酸与石灰石反应生成二氧化碳、水和氯化钙;稀盐酸与氢氧化钠反应生成水和氯化钠)
小刚和小洁以“化学反应中,反应物和生成物的质量关系”为课题进行科学探究,请填写以下探究过程中的空格:(提示:稀盐酸与石灰石反应生成二氧化碳、水和氯化钙;稀盐酸与氢氧化钠反应生成水和氯化钠)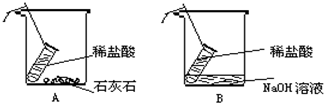 小刚和小洁以“化学反应中,反应物和生成物的质量关系”为课题进行科学探究,请填写以下探究过程中的空格:(提示:稀盐酸与石灰石反应生成二氧化碳和水、氯化钙;与氢氧化钠生成水和氯化钠)
小刚和小洁以“化学反应中,反应物和生成物的质量关系”为课题进行科学探究,请填写以下探究过程中的空格:(提示:稀盐酸与石灰石反应生成二氧化碳和水、氯化钙;与氢氧化钠生成水和氯化钠)