题目内容
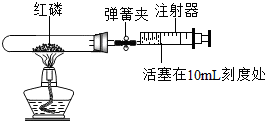
某同学用镁条代替红磷做空气中氧气含量测定实验,所用装置如图:
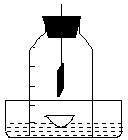
用蒸发皿来承接反应生成物。 ⑴.试分析该同学的实验设计的化学原理(用化学方程式表示)
⑵.实验时,将点燃的镁条迅速插入钟罩内,塞紧瓶塞,到冷却至室温后,发现钟罩内液面上升至2/5以上,该同学愕然了。你能分析出其中可能的原因吗? ___
⑶.取出蒸发皿,向其中固体中滴入水,迅速反应,产生刺激性气味的气体,用湿润的红色石蕊试纸试验,试纸变蓝色;分析此时蒸发皿中的物质,发现有一不溶碱。通过查阅资料得知:蒸发皿中的固体除氧化镁之外还有氮化镁(化学式为Mg3N2)请写出氮化镁与水反应的化学方程式:
⑷.如果改用木炭代替红磷做此实验,钟罩内水面上升最终将 1/5体积(填“大于”、“小于”或“等于”),如何改进此实验,使液面上升约为1/5体积 _______ ________
2Mg+O2 点燃 2Mg;可能是Mg和N2发生反应生成了固体;把水改成溶液NaOH或碱溶液。

练习册系列答案
相关题目
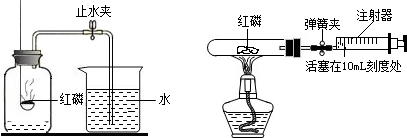
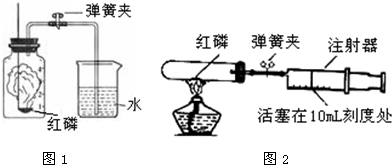
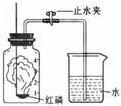 某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究.
某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究. 某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究.
某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究.