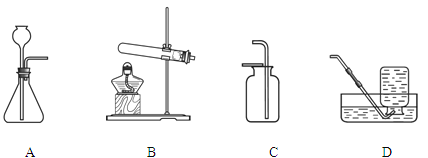
题目内容
【题目】根据下图回答问题。
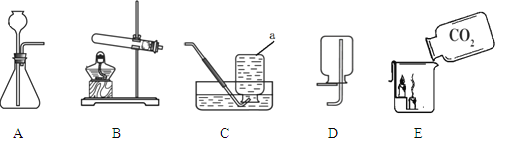
(1)实验室利用高锰酸钾制备氧气时,选用的发生和收集装置依次是(填字母序号)____________,化学反应方程式是________________。
(2)实验室利用装置_________制取二氧化碳,化学反应方程式是________________。E中观察到蜡烛自下而上依次熄灭,说明二氧化碳具有的物理性质________________。
【答案】(1)B、C 2KMnO4△K2MnO4+MnO2+O2↑
(2)A CaCO 3+2HCl== CaCl2 +CO2↑+H2O 密度比空气大
【解析】
试题分析:(1)气体发生装置的选择依据:反应物的状态和反应条件,实验室利用高锰酸钾制备氧气时,属于“固固加热型”,故发生装置选B,气体收集装置的选择依据:气体的密度和溶解性,由于氧气不易溶于水且密度比空气大,故收集装置选C;化学反应方程式是:2KMnO4==K2MnO4+MnO2+O2↑
(2)实验室制取二氧化碳是利用大理石和稀盐酸反应,属于“固液常温型”,故发生装置选A,化学反应方程式是:CaCO 3+2HCl△CaCl2 +CO2↑+H2O;E中观察到蜡烛自下而上依次熄灭,说明二氧化碳具有的物理性质:密度比空气大

【题目】某学习小组利用如图所示实验装置研究影响金属与硫酸反应速率的因素。
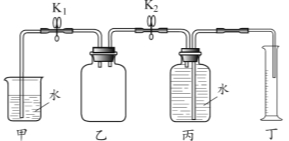
步骤如下:
① 关闭K2、打开K1,检查乙装置气密性,向乙中加入锌粒和稀硫酸,塞紧胶塞。
② 待气泡连续均匀产生,关闭K1、打开K2,并开始计时。
③ 待丁中收集到10 mL水,结束计时。
④ 换不同溶质质量分数、不同体积的硫酸,与质量相同的同一种锌粒重复实验。
每次实验的数据记录如下表:
实验 | 1 | 2 | 3 | 4 | 5 | 6 |
硫酸用量/mL | 10 | 20 | 40 | 10 | 20 | 40 |
硫酸的溶质质量分数/% | 10 | 10 | 10 | 20 | 20 | 20 |
收集所用时间/s | 106 | 102 | 97 | 45 | 41 | 40 |
(1)乙中发生反应的化学方程式为 。
(2)检查乙装置气密性的方法是 。
(3)通过比较实验_____________________(填数字)的数据可以得出,对金属与硫酸反应速率有显著影响的是 。