题目内容
3.2 g某物质在氧气中完全燃烧生成8.8gCO2和7.2gH2O,关于该物质的组成的判断有①一定含有C,H ②一定含O ③可能含O ④一定不含O ⑤分子中C,H的原子个数比为1:2 ⑥分子中C,H的原子个数比为1:4.其中正确的是
- A.①④⑥
- B.①②⑤
- C.①③⑤
- D.①④⑤
A
分析:根据二氧化碳中碳元素的质量分数和二氧化碳的质量计算出该物质中含有C元素的质量;根据水中氢元素的质量分数和水的质量计算出该物质中含有H元素的质量;因为该物质中含有C元素的质量+含有H元素的质量=该物质质量,故可判断,该物质中只含有含有C、H元素;然后假设C元素和H元素的个数,根据该物质中C元素和H元素的质量比即可计算出两者的比值.
解答:该物质中含有C元素的质量为:8.8g×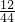 =2.4g;
=2.4g;
该物质中含有H元素的质量为:7.2g×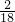 =0.8g;
=0.8g;
该物质中含有O元素的质量为:3.2g-2.4g-0.8g=0g;
故可判断该物质中一定含有C、H元素,一定不含O元素.
设C原子的个数为A,H的原子个数为B,则12A:B=2.4g:0.8g,
∴A:B=1:4.
故①④⑥是正确的.
故选A.
点评:本题主要考查学生运用化学式和元素的质量分数公式进行计算的能力.学生需认真分析已知条件,灵活运用计算方法,才能正确解答.
分析:根据二氧化碳中碳元素的质量分数和二氧化碳的质量计算出该物质中含有C元素的质量;根据水中氢元素的质量分数和水的质量计算出该物质中含有H元素的质量;因为该物质中含有C元素的质量+含有H元素的质量=该物质质量,故可判断,该物质中只含有含有C、H元素;然后假设C元素和H元素的个数,根据该物质中C元素和H元素的质量比即可计算出两者的比值.
解答:该物质中含有C元素的质量为:8.8g×
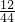 =2.4g;
=2.4g;该物质中含有H元素的质量为:7.2g×
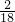 =0.8g;
=0.8g;该物质中含有O元素的质量为:3.2g-2.4g-0.8g=0g;
故可判断该物质中一定含有C、H元素,一定不含O元素.
设C原子的个数为A,H的原子个数为B,则12A:B=2.4g:0.8g,
∴A:B=1:4.
故①④⑥是正确的.
故选A.
点评:本题主要考查学生运用化学式和元素的质量分数公式进行计算的能力.学生需认真分析已知条件,灵活运用计算方法,才能正确解答.

练习册系列答案
相关题目