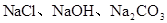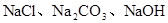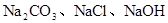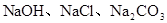题目内容
(2分)某学生为证明浓盐酸具有挥发性和碳酸具有不稳定性,设计了如下实验。
(1)将石灰石和浓盐酸反应产生的气体通入紫色石蕊试液,来证明浓盐酸的挥发性。
(2)将上述已变红的石蕊试液加热煮沸,就可证明碳酸已分解。试分析实验设计的是否合理,并说明理由。
实验一:
实验二:
(1)将石灰石和浓盐酸反应产生的气体通入紫色石蕊试液,来证明浓盐酸的挥发性。
(2)将上述已变红的石蕊试液加热煮沸,就可证明碳酸已分解。试分析实验设计的是否合理,并说明理由。
实验一:
实验二:
(1)不合理,石灰石和浓盐酸反应生成的二氧化碳也可以使紫色石蕊试液变红
(2)不合理,变红的石蕊试液加热煮沸红色变为紫色,也有可能是实验(1)中的氯化氢气体加热逸出所导致
(2)不合理,变红的石蕊试液加热煮沸红色变为紫色,也有可能是实验(1)中的氯化氢气体加热逸出所导致
(1)因为石灰石和浓盐酸反应生成氯化钙、二氧化碳和水,生成的二氧化碳也可以使紫色石蕊试液变红,所以此实验设计不合理;
(2)因为浓盐酸具有挥发性,挥发出的氯化氢气体也可以使紫色石蕊试液变红,加热后氯化氢气体会逸出,使得变红的石蕊试液重新变为紫色,所以此实验设计也不合理.
(2)因为浓盐酸具有挥发性,挥发出的氯化氢气体也可以使紫色石蕊试液变红,加热后氯化氢气体会逸出,使得变红的石蕊试液重新变为紫色,所以此实验设计也不合理.

练习册系列答案
相关题目

 三种金属离子,现用NaOH,
三种金属离子,现用NaOH, ,NaCl三种溶液使它们分别沉淀并分离出来,要求每次只加一种溶液,滤出一种沉淀,所加溶液顺序正确的是( )
,NaCl三种溶液使它们分别沉淀并分离出来,要求每次只加一种溶液,滤出一种沉淀,所加溶液顺序正确的是( )