题目内容
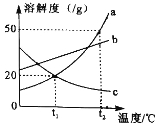
【题目】甲、乙两烧杯内盛有等质量、等质量分数的盐酸.将镁逐渐加入甲烧杯,铁逐渐加入乙烧杯,测量加入的金属质量m和相应的烧杯内物质质量变化量△m,画出△M﹣m曲线oac和obc的示意图,如图所示.根据图中信息,下列说法错误的是( )

A.m1:m2=3:7
B.m1﹣△M1<m2﹣△M2
C.曲线oac表示的是甲烧杯中△M与m的变化关系
D.当乙烧杯内加入铁的质量为m1时,溶液中溶质不止一种
【答案】B
【解析】
试题分析:镁与稀盐酸反应生成氯化镁和氢气,铁与稀盐酸反应生成氯化亚铁和氢气,反应的化学方程式分别是Mg+2HCl═MgCl2+H2↑、Fe+2HCl═FeCl2+H2↑.
Mg+2HCl═MgCl2+H2↑ △M1 Fe+2HCl═FeCl2+H2↑ △M2
24 2 24﹣2=22 56 2 56﹣2=54
A、由图示,m1、m2时金属与稀盐酸完全反应,由反应的化学方程式可知,参加反应的稀盐酸的质量相同时,此时消耗的镁与铁的质量比为24:56=3:7,正确;B、由题意,m1﹣△M1、m2﹣△M2即为金属质量与烧杯内物质质量变化量的差值,即生成氢气的质量,由反应的化学方程式,参加反应的盐酸的质量相等,则生成氢气的质量相等,即m1﹣△M1=m2﹣△M2,错误;C、由A选项的分析,完全反应时消耗的镁的质量少,则曲线oac表示的是甲烧杯中△M与m的变化关系,正确;D、当乙烧杯内加入铁的质量为m1时,稀盐酸有剩余,溶液中溶质不止一种,为氯化亚铁和HCl,正确。故选B

练习册系列答案
 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目