��Ŀ����
����Ŀ��Ԫ�����ڱ���ѧϰ�о���ѧ����Ҫ���ߣ��±���1��18��Ԫ�صIJ�����������ϼۺ�������ϼ۹�����Ϣ�� 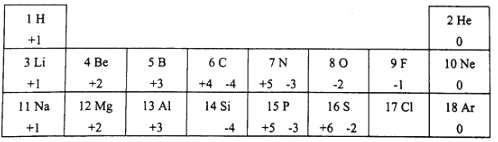
�������Ϣ���ش��������⣺
��1��12��Ԫ������Ԫ�أ���������ǽ���������������������дԪ�ط��ţ�ԭ�Ӿ�����ͬ�ĺ����������
��2�����в�ͬ��Ԫ����ʵ������� ��
��3������3��10��Ԫ��λ�ڵڶ����ڡ�11��18��Ԫ��λ�ڵ������ڣ���������ɿ�֪��ÿһ����Ԫ�غ������ͬ��9�ź�17��Ԫ��������������ͬ����������õ�����ʧȥ�������ӣ�
��4��17��Ԫ�ص�ԭ�Ӻ��������Ϊ �� �ƶϸ�Ԫ����������ϼ�Ϊ����������ϼ�Ϊ ��
���𰸡�
��1��������Ne
��2����������ͬ
��3���õ�
��4��17����1��
���������⣺��1��12��Ԫ����þԪ�����ڽ���Ԫ�أ�����ʧȥ���������������γ�����������������ԭ�Ӿ�����ͬ�ĺ�������������������Ne����2����ͬ��Ԫ����ʵ���������������ͬ�������������ͬ����3���ڶ����ڵ�3��10��Ԫ��ԭ�ӵĵ��Ӳ�����ͬ���������ڵ�11��18��Ԫ��ԭ�ӵĵ��Ӳ���Ҳ��ͬ����˵ó�����ÿһ����Ԫ��ԭ�ӵĵ��Ӳ�����ͬ�����Դ��ǣ����Ӳ�����
9�ź�17��Ԫ��������������ͬ����Ϊ7���ڻ�ѧ��Ӧ�ж��õ�һ�����Ӵﵽ�ȶ��ṹ������õ�����4��������ͬ�ĺ������������17��Ԫ�ص�ԭ�Ӻ��������Ϊ17����Ԫ����������ϼ�=����������=+7��������ϼ�=������������8=7��8=��1�����17��+7�ۣ���1�ۣ�

 ����ͼ���������������ϵ�д�
����ͼ���������������ϵ�д� ����ѧҵ���Ե�����ϵ�д�
����ѧҵ���Ե�����ϵ�д�����Ŀ�����ꡰ����������ȼ�ա���ʵ���ij��ȤС����һЩ�ɻ�����⣬���ǽ��������� 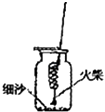
̽����
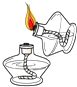
��1��������һ��ϸ��˿��������ȼ��Ϊʲô��������䣿
����������1������Ʒһ�㺬������̼����̼ϸ��˿ȼ��ʱ��̿�����ɵĶ�����̼������̬�������γ����ݣ�����̬����������ը�����������������
�����ʵ�顿Ϊ��̽���������������ԭ��С��ͬѧ��Ƶ�ʵ�鷽���ǣ� ��
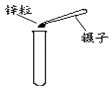
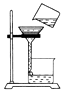
��ʵ��̽��1��С������ͼ��ʾװ����ϸ��˿��������ȼ�յ�ʵ�飮��������˿ȼ�գ�����ʵ���δ�ɹ���д�����¸�ͬѧʵ��ʧ�ܵĿ���ԭ������ ������
�����Ľ�����ͬѧ����˸�ʵ�飬д����Ӧ�����ֱ���ʽ ��
��2��������2����ȼ��ʱ���������ĺ�ɫ�����л���û������
����������2����Ȼ����������������Ҫ���������������������������֣�����������Ϊ����ɫ�������������ױ�����Ϊ��������������
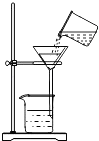
��ʵ��̽��2������ȴ��ĺ�ɫ�������飬 �� ˵�����������ĺ�ɫ�����л�������
��3��������3����ȼ�յIJ���Ϊʲô���������������أ�
����������3���������������������������ķֽ��¶ȼ��±������������������·ֽ������������
���������� | ���������� | �� | |
�ֽ��¶�/�� | 1538 | 1400 | ������ |
�ܵ�/�� | ������ | ������ | 1535 |
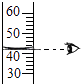
���������ۡ�����ʵ��������ϱ������ݣ�����֪����������ȼ��ʱ�����ĸ�����֮�䣬���¶ȷ�Χ�����������ѷֽ⣮
����չ���졿���������������·ֽ��������������һ�����壬д���÷�Ӧ�����ֱ���ʽ��
����Щ���е�ʳƷ��װ�з��к�ɫ������������ĩ������ĩ����ɫ �� ��˵����װ��©�����ۻ�Ա���ܼ�ʱ���ֲ�������