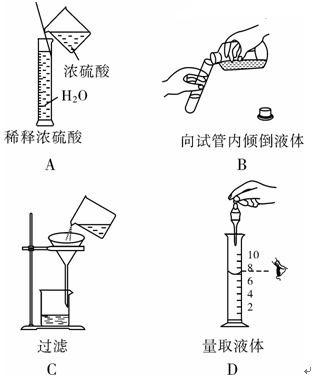
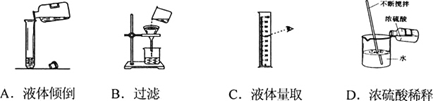
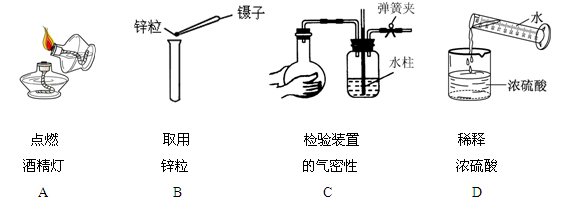
题目内容
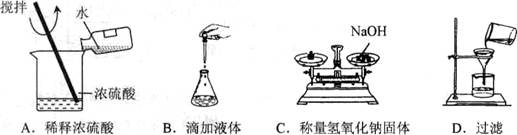
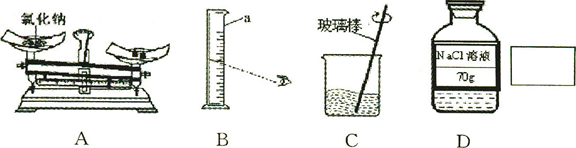
(7分)下列是小明同学配制100 g 10% NaCl溶液的实验操作示意图。
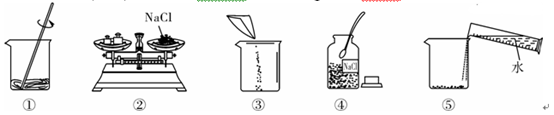
(1)该实验正确的操作顺序是____________(填序号)。
(2)认真观察指出图中错误的操作步骤________(填序号)。
(3)配制该溶液需要NaCl固体________g,需要水________mL(ρ水=1 g/mL)。
(4)小明同学将称量完毕的食盐转移到烧杯里时,不慎将少量食盐洒落在桌面上,这样会使所配制的溶液中溶质质量分数________10%(填“>”“=”或“<”)。
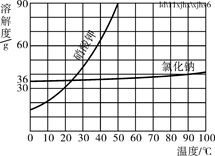
(5)部分物质溶解度曲线如右图所示,在20 ℃时,将40 g NaCl固体加入到100 g水中,搅拌使其充分溶解,你认为所得NaCl溶液的质量是________g,溶质质量分数是________%(精确到0.1%)。

(1)该实验正确的操作顺序是____________(填序号)。
(2)认真观察指出图中错误的操作步骤________(填序号)。
(3)配制该溶液需要NaCl固体________g,需要水________mL(ρ水=1 g/mL)。

(4)小明同学将称量完毕的食盐转移到烧杯里时,不慎将少量食盐洒落在桌面上,这样会使所配制的溶液中溶质质量分数________10%(填“>”“=”或“<”)。
(5)部分物质溶解度曲线如右图所示,在20 ℃时,将40 g NaCl固体加入到100 g水中,搅拌使其充分溶解,你认为所得NaCl溶液的质量是________g,溶质质量分数是________%(精确到0.1%)。
(1)④②③⑤① (2)② (3)10 90 (4)< (5)136 26.5
分析:(1)根据配制溶质质量分数一定的溶液的基本步骤考虑;(2)根据用天平称量物质的注意事项考虑;(3)溶质质量=溶液质量×溶质质量分数,溶剂质量=溶液质量-溶质质量;(4)根据溶质质量分数的计算方法考虑;(5)根据溶解度考虑加入的溶质是否全部溶解再进行计算.
解:(1)配制溶质质量分数一定的溶液的基本步骤:计算、称量、量取、溶解、装瓶存放;
(2)称量时左物右码,氯化钠不能直接放到托盘上;
(3)氯化钠质量:100g×10%=10g,需水:100g-10g=90g,水水体积: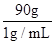 =90mL;
=90mL;
(4)不慎将少量食盐洒落在桌面上,溶质少了,导致溶质质量分数小了;
(5)20℃时,NaCl溶解度为36g说明100g水中最多溶36g,所以溶液质量为36g+100g=136g,溶质质量分数为: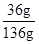 ×100%=26.5%
×100%=26.5%
故答案为:(1)④②③⑤①(2)②(3)10 90 (4)<(5)136 26.5
点评:本题容易出错的地方是要结合溶解度来看所加入的溶质是否全部溶解,不溶解的不能算溶液质量.
解:(1)配制溶质质量分数一定的溶液的基本步骤:计算、称量、量取、溶解、装瓶存放;
(2)称量时左物右码,氯化钠不能直接放到托盘上;
(3)氯化钠质量:100g×10%=10g,需水:100g-10g=90g,水水体积:
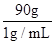 =90mL;
=90mL;(4)不慎将少量食盐洒落在桌面上,溶质少了,导致溶质质量分数小了;
(5)20℃时,NaCl溶解度为36g说明100g水中最多溶36g,所以溶液质量为36g+100g=136g,溶质质量分数为:
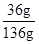 ×100%=26.5%
×100%=26.5% 故答案为:(1)④②③⑤①(2)②(3)10 90 (4)<(5)136 26.5
点评:本题容易出错的地方是要结合溶解度来看所加入的溶质是否全部溶解,不溶解的不能算溶液质量.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
 ×100%
×100%