题目内容
【题目】请结合如图回答问题。
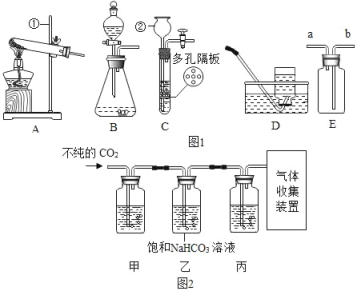
(1)仪器②的名称:_____。
(2)用氯酸钾和二氧化锰制取氧气,可选用装置_____(选填序号)和装置D组合,二氧化锰的作用是_____,若用B和D组合制取氧气,其反应的化学方程式为_____。
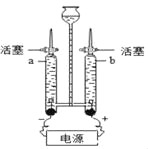
(3)实验室可用装置B或C制H2,C装置相对于B的优点有_____,用E装置收集H2,气体应从_____(选填“a”或“b”)端通入。若E中装满水,氢气从_____(选填“a”或“b”)端通入。
(4)某些大理石中含少量硫化物,使制得的CO2中混有H2S等气体。欲获取纯净、干燥的CO2,设计实验如下:
查阅资料:I.H2S能与NaOH、CuSO4等物质反应。
Ⅱ.CO2中混有的HCl气体可用饱和NaHCO3溶液吸收。
①装置甲中所盛试剂应选用_____(填字母)。
a浓硫酸 bNaOH溶液 c澄清石灰水 dCuSO4溶液
②装置丙的作用是_____。
【答案】长颈漏斗 A 催化作用 2H2O2![]() 2H2O+O2↑ 即开即停 a a d 干燥二氧化碳
2H2O+O2↑ 即开即停 a a d 干燥二氧化碳
【解析】
制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热。氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集。实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热。二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集。①装置甲中所盛试剂应选用CuSO4溶液除去硫化氢气体;②装置丙的作用是:干燥二氧化碳。
(1)长颈漏斗方便加液体药品,故答案为:长颈漏斗;
(2)如果用氯酸钾和二氧化锰制氧气就需要加热,其中二氧化锰起催化作用,故选A和装置D组合;如果用双氧水和二氧化锰制氧气就不需要加热,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平,化学方程式为![]() 。
。
(3)C装置相对于B的优点有:即开即停;用E装置收集H2,气体应从短管进入,故从a点进,因为氢气的密度比空气小;若E中装满水,氢气从短管进入,故从a点进,因为氢气的密度比水小。
(4)①装置甲中所盛试剂应选用CuSO4溶液除去硫化氢气体,故选用d装置;②装置丙的作用是:干燥二氧化碳。

【题目】碳还原氧化铜的实验如右图所示。写出该反应的化学方程式____。
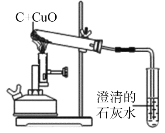
(提出问题)碳燃烧时可能生成CO2也可能生成CO,那么碳与氧化铜反应生成的气体是否也有多种可能?
(作出猜想)猜想①:CO
猜想②:CO2
想③:____________。
(设计方案)实验装置如图(浓硫酸具有吸水作用)。打开K,缓缓通入干燥的氮气一段时间,关闭K,点燃酒精喷灯和酒精灯,充分反应后,熄灭酒精喷灯和酒精灯,打开K,再通一段时间氮气。
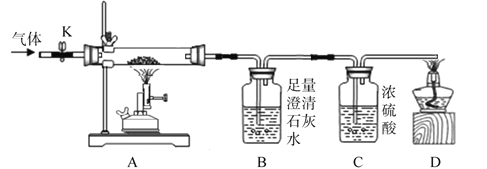
方案一:从定性观察角度判断
(1)实验时A处的现象是____________。
(2)若猜想①成立,B、D处的现象是_____________(填序号)。
a.B中变浑浊,D处能点燃 b.B中变浑浊,D处不能点燃
c.B中无明显实验现象,D处能点燃 d.B中无明显实验现象,D处不能点燃
方案二:从定量计算角度判断
取一定量炭粉和4g氧化铜的混合物进行实验,并测定表格中的四个数据:
反应前的质量 | 反应后的质量 | |
A(玻璃管+固体) | m1 | m2 |
B+C(广口瓶+混合液) | m3 | m4 |
(3)若猜想②成立,则理论上(m4-m3)__(m1-m2)(选填“<”、“>”或“=”)。
(4)若猜想③成立且CuO全部转化成Cu,则参加反应的碳的质量m的取值范围是____。
(交流反思)实验开始前缓缓通入氮气的目的是____。