题目内容
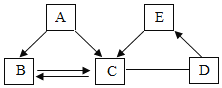
【题目】A、B、C、E均含有组成化合物种类最多的元素,其中A是单质;D、E均含有人体中含量最高的金属元素,其中E中该元素的质量分数为40%.它们之间的转化关系如图所示(“-”表示相连的物质能发生反应“→”表示一种物质能生成另一种物质,部分物质和反应条件已略去)。E的化学式为______;由C转化为B的反应条件是______,由D转化为E的化学方程式为______。
【答案】CaCO3 高温 CO2+Ca(OH)2=CaCO3↓+H2O
【解析】
D、E均含有人体中含量最多的金属元素,因此都含有钙元素;其中E是该元素的质量分数为40%,那么E是碳酸钙;A、B、C、E均含有组成化合物种类最多的元素,其中A是单质,因此A是碳;碳和氧气在点燃的条件下充分燃烧生成二氧化碳,不充分燃烧生成一氧化碳,因此B是一氧化碳,C是二氧化碳;二氧化碳和氢氧化钙反应生成碳酸钙白色沉淀和水,因此D是氢氧化钙,带入框图推断合理。
由分析可知:E是碳酸钙,化学式为CaCO3,由C转化为B是二氧化碳和碳反应生成一氧化碳,该反应条件是高温,由D转化为E的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O。

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案【题目】兴趣小组的同学利用提供的试剂:稀硫酸、澄清石灰水、氯化钠溶液、硫酸铜溶液和紫色石蕊溶液,探究酸碱盐的性质,小清同学将氯化钠溶液加入到稀硫酸中没有观察到明显现象,而将混合溶液加热一段时间后,意外地得到无色、有刺激性气味的气体.
(提出问题)刺激性气味的气体是什么?
(猜想与假设)猜想1.可能是二氧化硫;猜想2.可能是氯化氢;猜想3.可能是氨气
大家讨论后认为猜想3不合理,依据是_____.
(查阅资料)SO2和CO2的化学性质相似都能使澄清石灰水变浑浊,写出二氧化硫和氢氧化钙反应的化学方程式_____;
(实验探究)如图所示,小诚将产生的气体通入紫色石蕊溶液中,观察到_____,他认为猜想2正确.
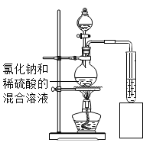
(评价与改进)小煜认为小诚的结论不科学,于是他利用提供的试剂通过实验确认了猜想2正确.
实验操作 | 实验现象 |
如图所示,将产生的气体_____ | 无明显现象 |
为进一步证明结论正确,他们又将该气体通入_____溶液中,观察到了预期的白色沉淀.
(结论)加热氯化钠和硫酸的混合物溶液得到的气体是氯化氢.
【题目】每年4、5月份是校园流感高发期,为此学校购买某品牌二氧化氯消毒液,如表为该消毒液的部分信息。
二氧化氯(ClO2)1000mL | |
溶质质量分数 | 80% |
密 度 | 1.2g/ml |
(1)二氧化氯(ClO2)中氯元素的化合价是_____。
(2)为预防流感,某校医务人员将其稀释至20%后,对全校教室进行全面消毒,从预防传染病的角度看,这属于_____(选“控制传染源”、“切断传播途径”或“保护易感人群”)。
(3)下列关于二氧化氯(ClO2)的说法正确的是_____。
A.二氧化氯由氯元素和氧元素组成
B.二氧化氯由二氧化氯分子构成
C.1个二氧化氯分子由1个氯原子和1个氧分子构成
D.二氧化氯中氯元素质量分数计算表达式为Cl%=![]() ×100%
×100%
(4)欲配制40kg质量分数为20%的稀二氧化氯消毒液,需要这种二氧化氯消毒液_____kg。
(5)当体内有炎症时会出现发热现象,这有利于吞噬细胞和杀菌物质等转移到炎症区,抵御病原体的攻击,此过程属于_____ (选“特异性免疫”或“非特异性免疫”)。