题目内容
盐碱湖中捞出来的纯碱中含有一定量的食盐,为测定其中碳酸钠的含量,化学小组的同学将某纯碱样品24.6g放入烧杯中,逐滴加入150g稀盐酸,恰好完全反应,待不再产生气泡时,得到168g的食盐溶液。计算原混合物中碳酸钠的质量分数和反应后溶液的溶质质量分数(CO2的溶解忽略不计)。
设: 原混合物中碳酸钠的质量为X ,生成氯化钠的质量为Y,生成二氧化碳的质量为z。
Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
106 117 44
X Y 6.6g
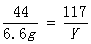
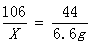
X=15.9g Y=17.6g
Na2CO3% =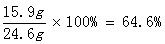
NaCl%=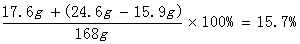
答:略

练习册系列答案
相关题目