题目内容
矿物燃料中常含有硫元素,在燃烧过程中会产生污染环境的SO2气体,该气体可用氢氧化钙悬浊液吸收,生成难溶于水的亚硫酸钙(CaSO3)和水.
(1)亚硫酸钙(CaSO3)的摩尔质量是________,其中Ca、S、O元素的原子个数比为________;1molCaSO3中约有________个硫原子.
(2)写出吸收SO2的化学反应方程式:________
(3)根据上述化学反应,若要吸收32g SO2气体,理论上需要________mol Ca(OH)2.
解:(1)当物质的质量以克为单位时,摩尔质量的单位为g/mol,在数值上等于该物质的相对原子质量或相对分子质量,所以亚硫酸钙(CaSO3)的摩尔质量为:40+32+16×3=120g/mol;
根据标在元素符号右下角的数字表示一个分子中所含原子的个数;因此CaSO3中Ca、S、O元素的原子个数比为:1:1:3;1molCaSO3中约有 6.02×1023 个硫原子.
故答案为:120g/mol; 1:1:3; 6.02×1023;
(2)氢氧化钙悬浊液吸收SO2的化学反应方程式为:SO2+Ca(OH)2=CaSO3+H2O 或 SO2+Ca(OH)2=CaSO3↓+H2O;
故答案为:SO2+Ca(OH)2=CaSO3+H2O 或 SO2+Ca(OH)2=CaSO3↓+H2O;
(3)先计算32g SO2为: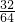 =0.5摩尔,
=0.5摩尔,
SO2+Ca(OH)2=CaSO3↓+H2O
1 1
0.5 X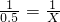 则 X=0.5 mol
则 X=0.5 mol
故答案为:0.5 mol.
分析:(1)根据单位物质的量的物质所具有的质量,称为摩尔质量,用符号M表示.当物质的质量以克为单位时,摩尔质量的单位为g/mol,在数值上等于该物质的相对原子质量或相对分子质量,进行解答;
根据标在元素符号右下角的数字表示一个分子中所含原子的个数;进行解答;
科学上把含有6.02×10^23个微粒的集体作为一个单位,叫摩尔;
(2)根据反应物与生成物和化学方程式的写配注等,写出反应化学方程式即可;
(3)先计算32g SO2为多少摩尔,根据方程式计算即可解答.
点评:本题考查了化学方程式的书写及摩尔质量的有关知识.
根据标在元素符号右下角的数字表示一个分子中所含原子的个数;因此CaSO3中Ca、S、O元素的原子个数比为:1:1:3;1molCaSO3中约有 6.02×1023 个硫原子.
故答案为:120g/mol; 1:1:3; 6.02×1023;
(2)氢氧化钙悬浊液吸收SO2的化学反应方程式为:SO2+Ca(OH)2=CaSO3+H2O 或 SO2+Ca(OH)2=CaSO3↓+H2O;
故答案为:SO2+Ca(OH)2=CaSO3+H2O 或 SO2+Ca(OH)2=CaSO3↓+H2O;
(3)先计算32g SO2为:
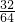 =0.5摩尔,
=0.5摩尔,SO2+Ca(OH)2=CaSO3↓+H2O
1 1
0.5 X
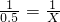 则 X=0.5 mol
则 X=0.5 mol故答案为:0.5 mol.
分析:(1)根据单位物质的量的物质所具有的质量,称为摩尔质量,用符号M表示.当物质的质量以克为单位时,摩尔质量的单位为g/mol,在数值上等于该物质的相对原子质量或相对分子质量,进行解答;
根据标在元素符号右下角的数字表示一个分子中所含原子的个数;进行解答;
科学上把含有6.02×10^23个微粒的集体作为一个单位,叫摩尔;
(2)根据反应物与生成物和化学方程式的写配注等,写出反应化学方程式即可;
(3)先计算32g SO2为多少摩尔,根据方程式计算即可解答.
点评:本题考查了化学方程式的书写及摩尔质量的有关知识.

练习册系列答案
相关题目