题目内容
【题目】在化学晚会上,小林同学表演了一个化学小魔术“空瓶生烟”(如图J3-7所示):A瓶中充满了氯化氢气体,B瓶中充满了氨气,抽出毛玻璃片,瓶中便充满了浓浓的白烟。请你根据所学知识回答下列问题:
![]()
(1)此现象说明了分子的哪个性质_________________
(2)若用“●”表示氢原子,用“![]() ”表示氮原子,用“
”表示氮原子,用“![]() ”表示氯原子,上述反应过程的微观模拟图如图所示。
”表示氯原子,上述反应过程的微观模拟图如图所示。
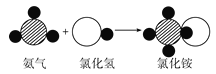
①该反应的化学方程式为__________________________________。
②氨气和氯化氢气体的化学性质________(填“相同”或“不同”)。分析以上微观模拟图,你能得出的结论是:____________________________(写一条)。
③该变化中的最小粒子是__________。
(3)如果两个瓶子是质地较软的塑料瓶,我们会观察到塑料瓶变瘪了,原因是________________________________________。
【答案】 分子在不断地运动 NH3 + HCl===== NH4Cl 不同 反应前后原子个数不变(其他合理答案均可) 氢原子、氮原子和氯原子 反应物为气体,生成物为固体,瓶内气体的体积减小,压强变小,瓶子变瘪
【解析】分析:(1)从分子在不断运动进行分析;
(2)由分子构成的物质,分子是保持物质化学性质的最小粒子,分子的种类不同,则构成物质的化学性质也不相同;原子是化学变化中的最小粒子;据此分析;
(3)从瓶内气体体积减小,压强变小,使瓶子变瘪进行分析。
解答:(1)由题意“A瓶中充满氯化氢气体,B瓶中充满氨气,抽开毛玻璃片,瓶中产生浓浓的白烟”,则知氯化氢和氨气发生反应,故知分子在不断运动;
(2)①![]() ;
;
②由分子构成的物质,分子是保持物质化学性质的最小粒子,分子的种类不同,则构成物质的化学性质也不相同;分析以上微观模拟图,能得出的结论是:反应前后原子个数不变。
③原子是化学变化中的最小粒子;故填:氢原子、氮原子和氯原子;
(3)固体分子之间的的间隔小于气体分子之间的间隔,故由气体生成固体时,体积变小,压强变小。
故答案为:(1). 分子在不断地运动 (2). ①![]() ② 不同;反应前后原子个数不变(其他合理答案均可) ③氢原子、氮原子和氯原子 (3). 反应物为气体,生成物为固体,瓶内气体的体积减小,压强变小,瓶子变瘪。
② 不同;反应前后原子个数不变(其他合理答案均可) ③氢原子、氮原子和氯原子 (3). 反应物为气体,生成物为固体,瓶内气体的体积减小,压强变小,瓶子变瘪。

【题目】常温下,小明同学在练习“金属的化学性质”实验操作时,发现几支试管中冒出气泡的速率有快有慢,于是他与小芳同学一起合作进行如下探究。
【提出问题】金属与酸反应的快慢受哪些因素影响呢?
【猜想与假设】A.可能与酸的浓度有关;B.可能与金属的种类有关;C.可能与金属的形状有关。
【设计并实验】小明和小芳进行如下实验。
实验 编号 | 盐酸的 浓度 | 金属 (均取2 g) | 金属的 形状 | 收集50 mL 氢气所需要 的时间/s |
① | 10% | 镁 | 粉状 | 60 |
② | 10% | 铁 | 片状 | 120 |
③ | 10% | 镁 | 片状 | 102 |
④ | 20% | 铁 | 片状 | 110 |
(1)实验时需将镁片和铁片进行打磨,其目的是______________________________________。
(2)写出铁与稀盐酸反应的化学方程式:________________________________。
【收集证据】
(3)要比较金属的种类对反应快慢的影响,应选择的实验编号是________。
【得出结论】通过上述四个实验,你得出的影响金属与酸反应的因素有________________________。
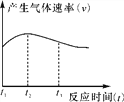
(4)实验①中试管外壁发烫,说明镁与稀盐酸反应是放热反应。实验测得该反应中产生气体的速率(v)与时间(t)的关系如图所示,你认为在t2~t3时间段内反应速率逐渐减慢的主要原因是________________________________________________________________________。