题目内容
【题目】实验室需配置质量分数为10%的氯化钠溶液进行实验,请看图完成以下问题: 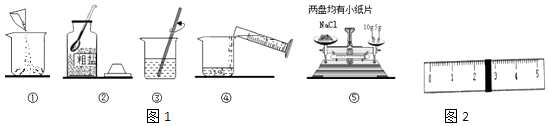
(1)若配制氯化钠溶液顺序如图1所示,正确的操作顺序是(用图中序号填空) , 其中玻璃棒的作用是 .
(2)称量NaCl时,天平平衡后的状态如图1⑤所示,游码标尺示数如图2,则称取的NaCl质量为 , 量取水的体积为(水的密度为1g/mL)
(3)量取水的体积时,该同学俯视读数,则会导致所配溶液的溶质质量分数会 . (“偏大”或“偏小”或“正常”).
【答案】
(1)②⑤①④③;搅拌加速溶解
(2)17.5g;157.5mL
(3)偏大
【解析】解:(1)配制溶质质量分数一定的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解,即②⑤①④③;玻璃棒搅拌的目的搅拌,加快氯化钠的溶解速率.(2)砝码的质量为10g+5g=15g,游码的质量为2.5g,所称取氯化钠的质量=15g+2.5g=17.5g;所配制溶液的质量= ![]() =175g,则需要水的质量=175g﹣17.5g=157.5g,由于水的密度是1g/mL,故需要水的体积为:157.5mL;故答案为:17.5g;157.5mL;(3)若量取水时俯视量筒量取的水体积偏小,溶质不变溶剂少了,所以溶质质量分数偏大.故答案为:偏大.
=175g,则需要水的质量=175g﹣17.5g=157.5g,由于水的密度是1g/mL,故需要水的体积为:157.5mL;故答案为:17.5g;157.5mL;(3)若量取水时俯视量筒量取的水体积偏小,溶质不变溶剂少了,所以溶质质量分数偏大.故答案为:偏大.
(1)配制溶质质量分数一定的溶液的基本步骤进行分析解答.根据溶解操作中玻璃棒的作用,进行分析解答;(2)砝码与游码的质量和为所称氯化钠的质量,游码读数时应以游码左侧数值为准;利用所称取溶质氯化钠的质量和所要配制溶液的溶质质质量分数,根据溶质质量分数计算公式,求出所要配制溶液的质量,溶液质量与溶质质量差即为溶剂水的质量,进而确定水的体积.(3)根据俯视读数量取的水的多少考虑溶质质量分数的变化.

【题目】A、在宏观、微观和符号之间建立联系是化学学科的特点. 甲、乙、丙、丁表示四种物质,它们的部分化学式和微观示意图分别列于表:
物质 | 甲 | 乙 | 丙 | 丁 | 图例: |
化学式 | H2O | C | ? | H2 | |
微观示意图 |
|
|
| ? |
(1)请你画出丁物质的微观示意图;
(2)构成甲物质的粒子是;
(3)四种物质中属于氧化物的是、(填化学式),请你从微观角度描述判断的依据: .

