题目内容
【题目】如图中的①、②分别是钠元素、氯元素在元素周期表中的信息,A、B、C是三种粒子的结构示意图。
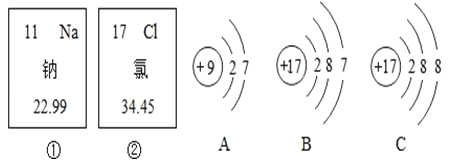
试回答下列问题:
(1)钠元素的原子序数为_____,其相对原子质量为_____,画出它的原子结构示意图_____;
(2)A的结构示意图中共有_____个电子层,最外层电子是_____,容易_____(填“得到”或“失去”)电子;
(3)A、B、C中属于同种元素的粒子是_____;
(4)A和B两种粒子的_____相同,所以它们具有相似的化学性质;
(5)A、B、C中达到稳定结构的是_____;
(6)钠原子和氯原子反应所形成的化合物是由_____(填“分子”“原子”或“离子”)构成的,化学式为_____。
【答案】11; 22.99;  2; 7; 得到 BC; 最外层电子数 C 离子; NaCl
2; 7; 得到 BC; 最外层电子数 C 离子; NaCl
【解析】
(1)由元素周期表的信息可知,钠元素的原子序数为11,其相对原子质量为22.99;其原子核内有11个质子,核外电子排布情况为2、8、1,所以钠原子结构示意图为 ;故填:
;故填:  ;
;
(2)由A粒子结构可知,A的结构示意图中共有2个电子层,最外层电子是7,容易得到电子;故填:2;7;得到;
(3)A、B、C中属于同种元素的粒子是BC,这是因为B和C中的核电荷数都是17,即都是氯元素;故填:BC;
(4)最外层电子数决定元素的化学性质,A和B两种粒子的最外层电子数相同,所以它们具有相似的化学性质;故填:最外层电子数;
(5)在C中的最外层为电子数为8,属于相对稳定结构;故填:C;
(6)在化学反应中,钠原子失去电子形成钠离子,氯原子得到电子形成氯离子,二者构成氯化钠,其化学式为NaCl;故填:离子;NaCl。

 名校课堂系列答案
名校课堂系列答案【题目】我国制碱工业的先驱侯德榜将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献.其生产工艺流程示意图如下:
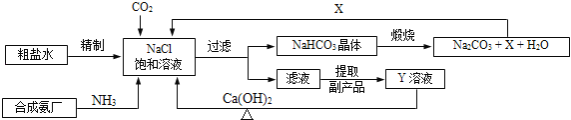
部分物质溶解性(室温) | |||
OH﹣ | SO42﹣ | CO32﹣ | |
Mg2+ | 不 | 溶 | 微 |
Ca2+ | 微 | 微 | 不 |
Ba2+ | 溶 | 不 | 不 |
(1)粗盐水中主要含有Ca2+、Mg2+、SO42﹣等杂质离子,工业上常用加入稍过量的NaOH溶液、Na2CO3溶液、BaCl2溶液及适量的盐酸等除杂、精制.则加入试剂合理的顺序为 、盐酸(只写一种).加盐酸的作用是(用化学方程式表示) 、 。
(2)制碱原理为:NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl,该反应原理可看作是由:①CO2+NH3+H2O=NH4HCO3和
②NaCl+NH4HCO3=NaHCO3↓+NH4Cl两个反应加合而成,则的反应类型为 .
(3)X的化学式为 .
(4)Y是滤液中最主要成分,Y与Ca(OH)2反应的产物之一可用于循环使用,该产物的名称为 ,Y的化学式为 ,写出Y的一种用途 。
【题目】某化学兴趣小组为了探究温度对H2O2分解反应速率的影响,借助如图所示实验装置,进行了两次实验,两次实验的部分设计如表所示:
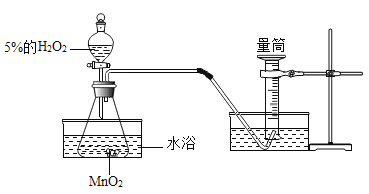
实验1 | 实验2 | |
MnO2的质量/克 | 0.5 | 0.5 |
5%的H2O2体积/毫升 | 40 | 待填 |
水浴温度/℃ | 20 | 80 |
温馨提示:本实验中的“水浴”是指通过水槽中的热水把热量传递到需要加热的锥形瓶里,达到加热的目的。
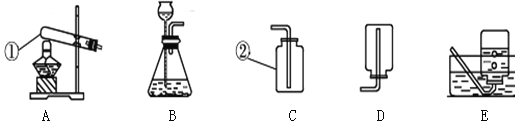
(1)该实验中收集气体的方法叫_____。
(2)实验2中“待填”的数据应为_____。
(3)实验结束后若要将MnO2从混合物中分离出来,可采取如下操作:_____、洗涤、干燥。
(4)在两次实验中,可通过_____来比较H2O2分解反应速率的大小。
(5)下列有关该实验的说法不正确的是_____。(填序号)
A 若俯视读数,则会导致测得的气体体积偏大
B 锥形瓶中原有的空气进入量筒会导致测得的气体体积偏大
C 实验过程中需待气泡连续且均匀产生时才能将导管伸到量筒口进行收集气体测定体积
D 实验2中由于温度较高使气体受热膨胀,会导致测得的分解速率比实际快