题目内容
【题目】下列说法正确的是( )
A.金属活动性 ![]()
B.Mn元素的化合价 ![]()
C.pH ![]()
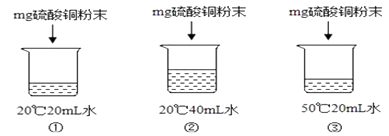
D.溶于水后的温度 ![]()
【答案】C
【解析】A、金属活动性由弱到强是金、银、铜、铁,A不符合题意;
B、钾显+1价,氧显-2价,根据在化合物中正负化合价代数和为零可知,K2MnO4、KMnO4、MnO2三者中Mn元素的化合价依次为+6、+7、+4,B不符合题意;
C、硝酸显酸性,NaCl溶液显中性,氨水显碱性,因此三者溶液的pH逐渐变大,C符合题意;
D、氧化钙与水反应放出大量的热,溶于水后的温度升高,氯化钠溶于水温度几乎不变,硝酸铵溶于水温度降低,D不符合题意;
所以答案是:C
【考点精析】本题主要考查了溶解时的吸热或放热现象和金属活动性顺序及其应用的相关知识点,需要掌握溶解时放热、吸热现象<溶解吸热:如NH4NO3溶解;溶解放热:如NaOH溶解、浓H2SO4溶解;解没有明显热现象:如NaCl>;在金属活动性顺序里:1、金属的位置越靠前,它的活动性就越强2、位于氢前面的金属能置换出盐酸、稀硫酸中的氢(不可用浓硫酸、硝酸)3、位于前面的金属能把位于后面的金属从它们的盐溶液中置换出来.(除K、Ca、Na)才能正确解答此题.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案
相关题目