题目内容
实验室需要配制50g溶质质量分数为4%的氢氧化钠溶液,所需固体氢氧化钠的质量为 g,主要操作步骤是:计算、 、溶解.在溶解过程中用玻璃棒搅拌,其作用是 .在量取水的过程中,某同学仰视读数,会使所配置的溶液中溶质质量分数 (填“偏大”“偏小”或“不变”).
| 利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;根据配制溶质质量分数一定的溶液的基本步骤进行分析解答; 玻璃棒的作用是:溶解时为加快溶解;用量筒量取水时,俯视液面,读数比实际液体体积大,会造成实际量取的水的体积偏小,据此进行分析判断对所配制的溶液中溶质质量分数的影响. | |
| 解答: | 解:实验室需要配制50g溶质质量分数为4%的氢氧化钠溶液,所需固体氢氧化钠的质量为50g×4%=2g. 配制一定质量分数的溶液的步骤:计算、称量(量取)、溶解. 在溶解操作中,玻璃棒起到搅拌以加快氢氧化钠溶解速率的作用. 用量筒量取水时,俯视液面,读数比实际液体体积大,会造成实际量取的水的体积偏小,则使所配制的溶液中溶质质量分数偏大. 故答案为:2;称量;加快氢氧化钠的溶解速率;偏大. |

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
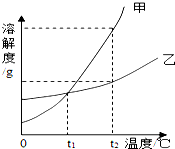 水和溶液在生产生活中重要的作用.
水和溶液在生产生活中重要的作用.