题目内容
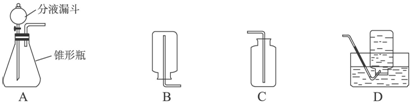
工业上用侯氏制碱法生产的纯碱中可能会混有NaCl、NH4Cl、FeCl3中的一种或几种.现按如图所示进行检验,出现的现象如图中所述.试根据实验过程和发生的现象回答下列问题:
(1)气体A的化学式为 ;沉淀B的颜色为 .
(2)若要证明气体E的成分,可将其通入 (填试剂名称).
(3)实验证明,溶液F中一定存在的溶质是(写化学式) .
(4)实验过程①中发生反应的化学方程式之一为 .
(5)实验步骤④的现象 (填“能”或者“不能”)证明NaCl一定混进了纯碱样品,请说出判断的理由: .

(1)气体A的化学式为
(2)若要证明气体E的成分,可将其通入
(3)实验证明,溶液F中一定存在的溶质是(写化学式)
(4)实验过程①中发生反应的化学方程式之一为
(5)实验步骤④的现象
考点:物质的鉴别、推断,盐的化学性质,铵态氮肥的检验,书写化学方程式、文字表达式、电离方程式
专题:混合物组成的推断题
分析:根据题中所给的各种物质都溶于水,氯化铵和氢氧化钠反应会生成氯化钠、水和氨气,氢氧根离子和铁离子会生成红褐色的氢氧化铁沉淀,氨气能使湿润的红色石蕊试纸变蓝色,氯离子和银离子会生成白色的氯化银沉淀等知识进行分析.
解答:解:题中所给的各种物质都溶于水,氯化铵和氢氧化钠反应会生成氯化钠、水和氨气,氢氧根离子和铁离子会生成红褐色的氢氧化铁沉淀,氨气能使湿润的红色石蕊试纸变蓝色,氯离子和银离子会生成白色的氯化银沉淀.
纯碱样品加入过量的氢氧化钠溶液,生成的气体A能使红色石蕊试纸变蓝色,所以A是氨气,混合物中一定含有氯化铵,氢氧化钠和氯化铁反应会生成红褐色的氢氧化铁沉淀和氯化钠,所以混合物中一定含有氯化铁,沉淀B是红褐色的氢氧化铁沉淀,溶液C中行含有碳酸钠、氯化钠和反应剩余的氢氧化钠,加入适量的稀硝酸,所以E是二氧化碳,溶液D中含有氯化钠和硝酸钠,氯化钠和硝酸银反应会生成氯化银沉淀和硝酸钠,所以G是氯化银,F中含有硝酸钠,所以
(1)气体A的化学式为NH3,沉淀B的颜色为红褐色;
(2)通过推导可知E是二氧化碳,检验二氧化碳,一般用澄清石灰水,所以要证明气体E的成分,可将其通入澄清石灰水;
(3)通过实验证明,溶液F中一定存在的溶质是NaNO3;
(4)氯化铵和氢氧化钠反应生成氯化钠、水和氨气,化学方程式为:NH4Cl+NaOH=NaCl+H2O+NH3↑;
(5)氢氧化钠和氯化铁反应会生成氢氧化铁沉淀和氯化钠,氢氧化钠和氯化铵反应会生成氯化钠、水和氨气,所以实验步骤④的现象不能证明NaCl一定混进了纯碱样品,判断的理由是:氯化铵、氯化铁和氢氧化钠反应生成氨气的同时也生成了氯化钠,所以无法判断是混合物中的氯化钠,还是生成的氯化钠生成的沉淀.
故答案为:(1)NH3,红褐色;
(2)澄清石灰水;
(3)NaNO3;
(4)NH4Cl+NaOH=NaCl+H2O+NH3↑;
(5)不能,氯化铵、氯化铁和氢氧化钠反应生成氨气的同时也生成了氯化钠,所以无法判断是混合物中的氯化钠,还是生成的氯化钠生成的沉淀.
纯碱样品加入过量的氢氧化钠溶液,生成的气体A能使红色石蕊试纸变蓝色,所以A是氨气,混合物中一定含有氯化铵,氢氧化钠和氯化铁反应会生成红褐色的氢氧化铁沉淀和氯化钠,所以混合物中一定含有氯化铁,沉淀B是红褐色的氢氧化铁沉淀,溶液C中行含有碳酸钠、氯化钠和反应剩余的氢氧化钠,加入适量的稀硝酸,所以E是二氧化碳,溶液D中含有氯化钠和硝酸钠,氯化钠和硝酸银反应会生成氯化银沉淀和硝酸钠,所以G是氯化银,F中含有硝酸钠,所以
(1)气体A的化学式为NH3,沉淀B的颜色为红褐色;
(2)通过推导可知E是二氧化碳,检验二氧化碳,一般用澄清石灰水,所以要证明气体E的成分,可将其通入澄清石灰水;
(3)通过实验证明,溶液F中一定存在的溶质是NaNO3;
(4)氯化铵和氢氧化钠反应生成氯化钠、水和氨气,化学方程式为:NH4Cl+NaOH=NaCl+H2O+NH3↑;
(5)氢氧化钠和氯化铁反应会生成氢氧化铁沉淀和氯化钠,氢氧化钠和氯化铵反应会生成氯化钠、水和氨气,所以实验步骤④的现象不能证明NaCl一定混进了纯碱样品,判断的理由是:氯化铵、氯化铁和氢氧化钠反应生成氨气的同时也生成了氯化钠,所以无法判断是混合物中的氯化钠,还是生成的氯化钠生成的沉淀.
故答案为:(1)NH3,红褐色;
(2)澄清石灰水;
(3)NaNO3;
(4)NH4Cl+NaOH=NaCl+H2O+NH3↑;
(5)不能,氯化铵、氯化铁和氢氧化钠反应生成氨气的同时也生成了氯化钠,所以无法判断是混合物中的氯化钠,还是生成的氯化钠生成的沉淀.
点评:在解此类题时,首先分析所给混合物中各物质的性质,然后根据题中所给的实验现象进行判断,最后确定混合物的组成成分.

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
根据下列四种粒子的结构示意图,所获取的信息正确的是( )
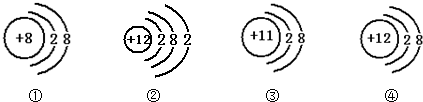

| A、它们表示四种元素 |
| B、②表示的元素在化合物中通常显+2价 |
| C、④表示的元素是非金属元素 |
| D、①③④表示的是阳离子 |
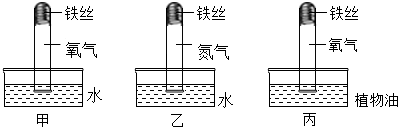
 如图是某同学做质量守恒定律的验证实验装置,他用白磷燃烧,试根据要求完成下列问题:
如图是某同学做质量守恒定律的验证实验装置,他用白磷燃烧,试根据要求完成下列问题: 小明同学在实验室发现了一瓶敞口放置的过氧化氢溶液,他认为该溶液中溶质的质量分数减小了,需要重新测定并更换试剂瓶的标签.他做了如图实验:称量该溶液34.0g倒入烧杯中,然后向其中加入0.5g二氧化锰,直到不再放出气体后,再称量烧杯中混合物的质量,称量结果为32.9g.
小明同学在实验室发现了一瓶敞口放置的过氧化氢溶液,他认为该溶液中溶质的质量分数减小了,需要重新测定并更换试剂瓶的标签.他做了如图实验:称量该溶液34.0g倒入烧杯中,然后向其中加入0.5g二氧化锰,直到不再放出气体后,再称量烧杯中混合物的质量,称量结果为32.9g.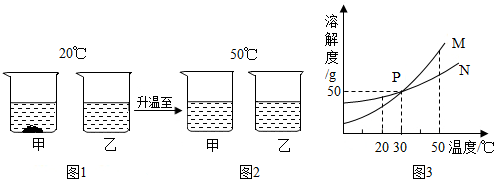
 如图是A、B两物质(均不含结晶水)的溶解曲线,据此回答以下问题:
如图是A、B两物质(均不含结晶水)的溶解曲线,据此回答以下问题: