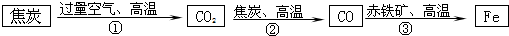题目内容
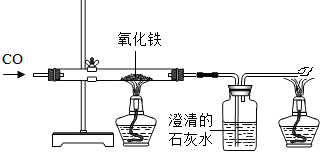
27、钢铁是重要的金属材料.
(1)下列铁制品中利用了铁的延展性的是

(2)目前世界上已有50%以上的废钢铁得到回收利用,其目的是
A.节约金属资源 B.合理开采矿物 C.防止钢铁生锈
(3)为防止水龙头生锈,其表面镀有一层铬.铁生锈的条件是
(4)在研究铁的性质实验后,某实验室废液桶中收集了溶解大量FeSO4、CuSO4的废液.小军准备运用学到的有关化学知识对废液进行处理.他设计除去铜离子,回收硫酸亚铁晶体和铜的实验方案,请你参与讨论有关问题:
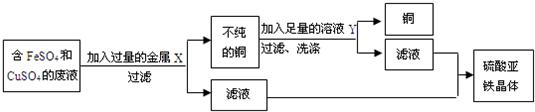
①预处理.废水在加入金属X前先进行过滤,目的是除去
②金属X是
溶液Y是
(1)下列铁制品中利用了铁的延展性的是
C
.
(2)目前世界上已有50%以上的废钢铁得到回收利用,其目的是
A
.A.节约金属资源 B.合理开采矿物 C.防止钢铁生锈
(3)为防止水龙头生锈,其表面镀有一层铬.铁生锈的条件是
与水和氧气接触
.(4)在研究铁的性质实验后,某实验室废液桶中收集了溶解大量FeSO4、CuSO4的废液.小军准备运用学到的有关化学知识对废液进行处理.他设计除去铜离子,回收硫酸亚铁晶体和铜的实验方案,请你参与讨论有关问题:

①预处理.废水在加入金属X前先进行过滤,目的是除去
不溶物
.②金属X是
Fe(或铁)
,其加入废液后发生反应的化学方程式为Fe+CuSO4=FeSO4+Cu
;溶液Y是
稀硫酸
,利用其除去铜中杂质,有关反应的化学方程式为Fe+H2SO4=FeSO4+H2↑
.分析:根据金属的共性硬度、延展性、导热性和回收金属的目的来解答;根据铁锈蚀的条件与空气中的水和氧气同时接触来解答;根据题干中的反应物,生成物来写方程式及判断反应物.
解答:解:
(1)铁锤和水龙头利用了硬度大等性质,铁丝利用了延展性,炊具是利用其导热性的,故选C;
(2)回收利用金属是为了节约金属资源,故选A;
(3)铁与空气中的水和氧气同时接触易生锈,故填:与水和氧气接触;
(4)根据金属的活动顺序,排在前面的金属可以把排在后面的金属从它的盐溶液中置换出来,加入的X为铁,化学方程式:Fe+CuSO4=FeSO4+Cu;只有排在氢前面的金属可以和酸反应生成氢气,溶液Y为稀硫酸,化学方程式:Fe+H2SO4=FeSO4+H2↑.
故答案为:(1)C(2)A(3)与水和氧气接触(4)①不溶物②Fe(或铁)、Fe+CuSO4=FeSO4+Cu、稀硫酸、Fe+H2SO4=FeSO4+H2↑.
(1)铁锤和水龙头利用了硬度大等性质,铁丝利用了延展性,炊具是利用其导热性的,故选C;
(2)回收利用金属是为了节约金属资源,故选A;
(3)铁与空气中的水和氧气同时接触易生锈,故填:与水和氧气接触;
(4)根据金属的活动顺序,排在前面的金属可以把排在后面的金属从它的盐溶液中置换出来,加入的X为铁,化学方程式:Fe+CuSO4=FeSO4+Cu;只有排在氢前面的金属可以和酸反应生成氢气,溶液Y为稀硫酸,化学方程式:Fe+H2SO4=FeSO4+H2↑.
故答案为:(1)C(2)A(3)与水和氧气接触(4)①不溶物②Fe(或铁)、Fe+CuSO4=FeSO4+Cu、稀硫酸、Fe+H2SO4=FeSO4+H2↑.
点评:此题是一道综合性题目,但并不难,需结合所学知识和题干信息仔细分析,从而作答

练习册系列答案
相关题目

 钢铁是重要的金属材料,在建造淮安涟水飞机场时就是用了大量的钢铁.
钢铁是重要的金属材料,在建造淮安涟水飞机场时就是用了大量的钢铁.