题目内容
100g某硫酸溶液恰好与6.5g锌完全反应.这种硫酸溶液中溶质的质量分数是多少?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:欲求这种硫酸的溶质质量分数,需先求出参加反应的H2SO4的质量,再根据溶质质量分数=
×100%计算即可.
| 溶质质量 |
| 溶液质量 |
解答:解:设参加反应的H2SO4的质量为x
Zn+H2SO4=ZnSO4+H2↑
65 98
6.5g x
=
x=9.8g
这种硫酸溶液中溶质的质量分数是
×100%=9.8%
答案:这种硫酸溶液中溶质的质量分数是9.8%
Zn+H2SO4=ZnSO4+H2↑
65 98
6.5g x
| 65 |
| 98 |
| 6.5g |
| x |
x=9.8g
这种硫酸溶液中溶质的质量分数是
| 9.8g |
| 100g |
答案:这种硫酸溶液中溶质的质量分数是9.8%
点评:本题主要考查学生对物质质量分数和溶质质量分数的计算能力.学生需正确书写出化学方程式,并能正确运用溶质质量分数公式进行计算,才能正确答题.

练习册系列答案
相关题目
对下列物质在氧气中燃烧的实验现象描述正确的是( )
| A、石蜡在氧气中燃烧时,有水和二氧化碳生成 |
| B、铝箔在氧气中燃烧时,发出耀眼的白光,生成白色固体 |
| C、红磷在氧气中燃烧时,生成一种红色固体 |
| D、铁丝在氧气中燃烧时,火星四射,生成白色固体 |
以下做法错误的是( )
| A、食用瘦肉等含铁食物预防缺铁性贫血 |
| B、用聚氯乙烯塑料制成食品保鲜膜 |
| C、用二氧化碳灭火器扑灭图书、档案等物的失火 |
| D、医疗上用氯化钠配制生理盐水 |
维生素C(C6H8O6)主要存在于蔬菜、水果中,它能促进人体生长发育、增强人体对疾病的抵抗能力,近年科学家还发现维生素C有防癌作用.下列关于维生素C的说法中错误的是( )
| A、维生素C由碳、氢、氧三种元素组成 |
| B、维生素C中C、H、O三种元素的质量比是3:4:3 |
| C、维生素C的相对分子质量是176 |
| D、一个维生素C分子由6个碳原子、8个氢原子、6个氧原子构成 |

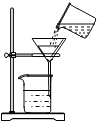 我市某化学兴趣小组的同学用洁净的塑料瓶从釜溪河中取回一定量的水样,然后进行如下研究分析:
我市某化学兴趣小组的同学用洁净的塑料瓶从釜溪河中取回一定量的水样,然后进行如下研究分析: