题目内容
【题目】盐能与许多物质发生复分解反应,请分析下列化学反应,并回答问题:
① BaCl2 + H2SO4 = 2HCl +BaSO4↓
② CuSO4 + 2NaOH = Na2SO4 + Cu(OH)2↓
(1)从反应物的类型①是盐与酸的反应,②是盐与_________的反应。
(2)从复分解反应发生的条件分析,①和②都能反应的原因是生成物中都有__________。
(3)氯化钠俗名食盐,它的溶液也能跟____________ 溶液发生复分解反应,符合盐与盐之间的反应规律。
(4)在生活中纯碱(碳酸钠)是一种重要的盐,它与稀盐酸也能发生复分解反应。如果向5.3g碳酸钠粉末中,缓缓加入100g稀盐酸,若恰好完全反应。试计算:反应前稀盐酸中溶质的质量分数_________。
【答案】碱 沉淀 硝酸银 3.65%
【解析】
(1)从反应物的类型①为氯化钡与稀硫酸的反应,是盐与酸的反应,②硫酸铜与氢氧化钠的反应,是盐与碱的反应。
(2)复分解反应发生的条件为有沉淀、气体或水生成,从复分解反应发生的条件分析,①和②都能反应的原因是生成物中都有沉淀。
(3)氯化钠俗名食盐,它的溶液也能跟硝酸银溶液发生复分解反应生成氯化银沉淀和氯化钠,符合盐与盐之间的反应规律。
(4)向5.3g碳酸钠粉末中,缓缓加入100g稀盐酸,恰好完全反应,设参加反应的HCl的质量为x,则有:
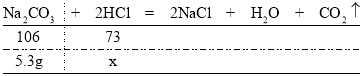
由![]() 解得x=3.65g
解得x=3.65g
稀盐酸中溶质的质量分数为![]()
答:稀盐酸中溶质的质量分数为3.65%。

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
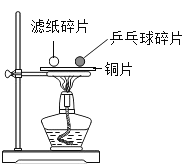
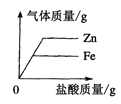
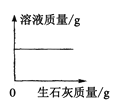
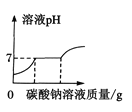
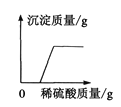
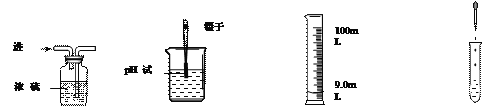
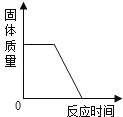
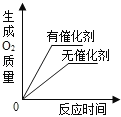
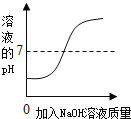
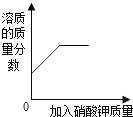
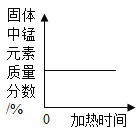
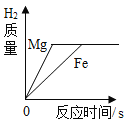
【题目】下列四个图像中,能正确反映对应变化关系的是 ( )
|
|
|
|
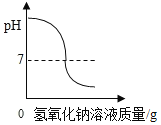
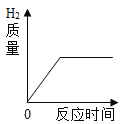
A.加热一定量的高锰酸钾固体 | B.向两份完全相同的硫酸中,分别加入过量的铁粉和镁粉 | C.向稀盐酸中滴加氢氧化钠溶液 | D.将生锈严重的铁钉,放入到足量的稀盐酸中 |
A.AB.BC.CD.D