题目内容
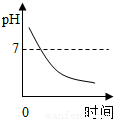
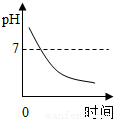
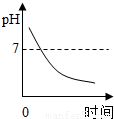
某种消化药片的有效成分氢氧化镁,能减缓因胃酸过多引起的疼痛.在氢氧化镁与胃酸作用的过程中,胃液pH变化的情况是( )A.
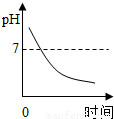
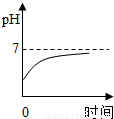
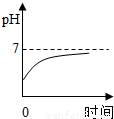
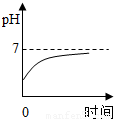
B.
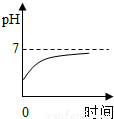
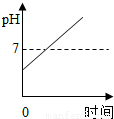
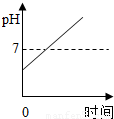
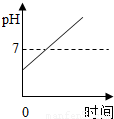
C.
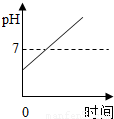
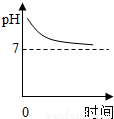
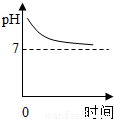
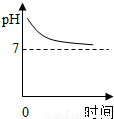
D.
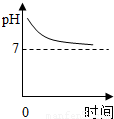
【答案】分析:根据氢氧化镁、盐酸以及它们反应后的生成物的pH值来判断胃液中pH值的变化.
解答:解:胃液中含有盐酸,所以胃液中的pH值小于7,当服用含有氢氧化镁的药片后胃液中的盐酸要和氢氧化镁反应,所以溶液的pH值要增大,但是由于服用的药片是适量的,所以只能中和一部分盐酸,故胃液的pH值依然为小于7,因为在酸性的环境中利于食物的消化.故选项B是正确的.
故选B.
点评:本题是考查了中和反应的应用,向酸中加入碱性物质时,溶液的pH会升高,在运用这一原理解决问题时要考虑实际,例如本题中服用的药片应该是适量的,因为这是治疗人类疾病.
解答:解:胃液中含有盐酸,所以胃液中的pH值小于7,当服用含有氢氧化镁的药片后胃液中的盐酸要和氢氧化镁反应,所以溶液的pH值要增大,但是由于服用的药片是适量的,所以只能中和一部分盐酸,故胃液的pH值依然为小于7,因为在酸性的环境中利于食物的消化.故选项B是正确的.
故选B.
点评:本题是考查了中和反应的应用,向酸中加入碱性物质时,溶液的pH会升高,在运用这一原理解决问题时要考虑实际,例如本题中服用的药片应该是适量的,因为这是治疗人类疾病.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目