题目内容
铁是人们广泛使用的金属,下列关于铁的说法正确的是
- A.铁是地壳里含量最多的金属元素
- B.人类历史上铁器的使用早于铜器
- C.纯净的生铁属于金属单质
- D.生铁和钢都是铁的合金
D
地壳中元素含量居前五位的元素是:O、Si、Al、Fe、Ca、Fe是第二位的金属元素,A项错误;在商朝时期开始使用铜器,而在春秋战闰时期冶铁炼钢,铜器早于铁器,故B项错误;生铁是一种铁合金,含碳量2%~4.3%,还含少量硅、锰、硫、磷等,故C错误.
有的同学易误选C,是因为只看到“纯净”二字,而未深入分析“合金”,合金是混合物,如同“纯净的空气”或“净化后的空气”均是混合物,不要被“纯净”两字迷惑.
地壳中元素含量居前五位的元素是:O、Si、Al、Fe、Ca、Fe是第二位的金属元素,A项错误;在商朝时期开始使用铜器,而在春秋战闰时期冶铁炼钢,铜器早于铁器,故B项错误;生铁是一种铁合金,含碳量2%~4.3%,还含少量硅、锰、硫、磷等,故C错误.
有的同学易误选C,是因为只看到“纯净”二字,而未深入分析“合金”,合金是混合物,如同“纯净的空气”或“净化后的空气”均是混合物,不要被“纯净”两字迷惑.

练习册系列答案
相关题目
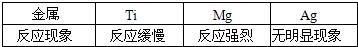
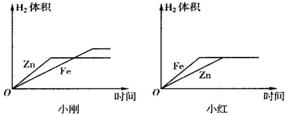
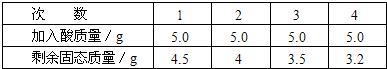
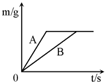 金属材料用途广泛,回答下列问题:
金属材料用途广泛,回答下列问题:

