题目内容
查资料可知,在化学反应中元素化合价升高的物质做还原剂。定向爆破常伴有反应: 2Al+Fe2O3 Al2O3+2Fe,此反应中还原剂是:
Al2O3+2Fe,此反应中还原剂是:
| A.Al | B.Fe | C.Fe2O3 | D.Al2O3 |
A
解析试题分析:根据反应物的得氧和失氧来判断,得氧的是还原剂,失氧的是氧化剂;故在化学反应2Al+Fe2O3 Al2O3+2Fe中,铝得氧是还原剂,氧化铁失氧是氧化剂。故选A
Al2O3+2Fe中,铝得氧是还原剂,氧化铁失氧是氧化剂。故选A
考点:氧化还原反应
点评:熟记氧化还原反应的特点,是解题的关键,要能从反应物的得氧和失氧的角度来分析判断。

根据下列实验装置图,回答问题。
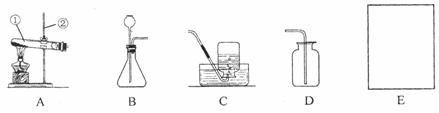
(1)写出上图中标有序号的仪器名称:①___________,②___________。
(2)利用A装置制取氧气反应的文字表达式为___________;其中A装置中试管口略向下倾斜的目的是___________;在进行制取氧气的操作时,加入药品之前必须进行的一步操作是___________。
(3)查阅资料:相同条件下,氨气(NH3)的密度比空气小,且易溶于水,其水溶液称为氨水;加热氯化铵和氢氧化钙固体混合物可制取氨气。
根据所查资料,制取氨气应选择的收集装置是___________(填序号,如果没有合适选项请选E并在方框中画出合适的装置)。
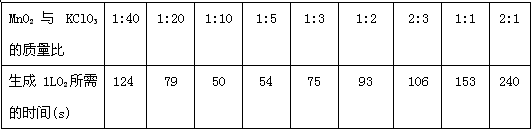
(4)下表是某同学利用氯酸钾和二氧化锰制取氧气时测定的实验数据。
| MnO2与KClO3的质量比 | 1:40 | 1:20 | 1:10 | 1:5 | 1:3 | 1:2 | 2:3 | 1:1 | 2:1 |
| 生成1LO2所需的时间(s) | 124[来源:学科网] | 79 | 50 | 54 | 75 | 93 | 106 | 153 | 240 |
①据上表可知二氧化锰与氯酸钾的质量比为___________时,反应速率最快;
②二氧化锰的用量过少时产生氧气的速率很慢,可能原因是___________;
③通过上述数据分析可知,在化学反应中催化剂的用量___________
(填“是”或“不是”)越多越好。

 锰酸钾+二氧化锰+氧气
锰酸钾+二氧化锰+氧气
 Al2O3+2Fe,此反应中还原剂是:
Al2O3+2Fe,此反应中还原剂是: