题目内容
如图是a、b、c三种固体物质的溶解度曲线.下列说法中不正确的是( )
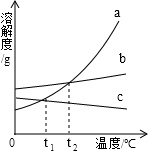

| A、在t2℃时,a的溶解度等于b的溶解度 | B、c的饱和溶液由t1℃升温至t2℃时,变成不饱和溶液 | C、在t1℃时,a、c饱和溶液中溶质的质量分数相同 | D、当a中含有少量b时,可以用降温结晶的方法提纯a |
分析:溶解度曲线中交点的意义是该温度下,两种物质的溶解度相等;饱和溶液中溶质的质量分数=
×100%;对于陡升型物质可以用降温结晶的方法得到晶体.
| 溶解度 |
| 溶解度+100g |
解答:解:A、由图可知,在t2℃时,曲线a与b相交,a的溶解度等于b的溶解度,故A正确;
B、c物质的溶解度随温度的升高而减小,所以c的饱和溶液由t1℃升温至t2℃时,会析出晶体,溶液仍为饱和溶液,故B不正确;
C、由图可知,在t1℃时,a、c两物质的溶解度相等,根据饱和溶液中溶质的质量分数=
×100%,可求出在t1℃时,a、c饱和溶液中溶质的质量分数相同,故C正确;
D、a为陡升型物质,b为缓升型物质,所以当a中含有少量b时,可以用降温结晶的方法提纯a,故D正确.
故选B
B、c物质的溶解度随温度的升高而减小,所以c的饱和溶液由t1℃升温至t2℃时,会析出晶体,溶液仍为饱和溶液,故B不正确;
C、由图可知,在t1℃时,a、c两物质的溶解度相等,根据饱和溶液中溶质的质量分数=
| 溶解度 |
| 溶解度+100g |
D、a为陡升型物质,b为缓升型物质,所以当a中含有少量b时,可以用降温结晶的方法提纯a,故D正确.
故选B
点评:本题综合考查溶解度曲线的意义,要求我们灵活掌握溶解度与溶质质量分数的关系,同时明确对于不同种类的物质可以采用不同的结晶方法.

练习册系列答案
相关题目
 17、如图是A、B、C三种固体物质的溶解度曲线示意图,试回答下列问题.
17、如图是A、B、C三种固体物质的溶解度曲线示意图,试回答下列问题. 29、如图是a、b、c三种固体物质的溶解度曲线图.
29、如图是a、b、c三种固体物质的溶解度曲线图. 16、如图是A、B、C三种固体物质的溶解度随温度变化的曲线图.根据图回答:
16、如图是A、B、C三种固体物质的溶解度随温度变化的曲线图.根据图回答: (1)如图是A、B、C三种物质的溶解度曲线.请回答:
(1)如图是A、B、C三种物质的溶解度曲线.请回答:
