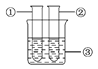
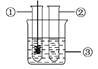
��Ŀ����
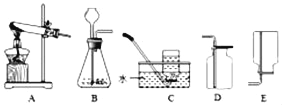
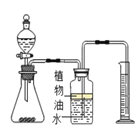
����Ŀ��ʵ���ҳ�������װ����ȡ���壬���������ѧ֪ʶ�ش���������
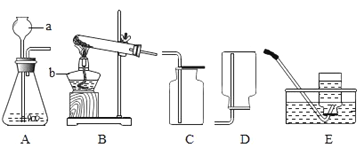

��1��д�����a��b���������ƣ�a____________��b_____________��
��2���ø��������ȡO2��װ��B��������һ��Ķ���________���������� _________________________��д����Ӧ�����ֻ���ű���ʽ_______________________��������ijͬѧ���ʵ�����ø��������ȡ�����IJ���ʵ����������в���������_______________��������ĸ��ţ�
A���ȼ��װ�õ������ԣ����ҩƷ B���ȹ̶��Թܣ�����þƾ���
C���Ƚ��������뼯��ƿ��������Թ� D������ʱ��Ԥ�ȣ��ټ��м���
��3��ijͬѧ����ˮ�������ռ���һƿ�����������飬������������������������Ŀ���ԭ����_________������ĸ��ţ���
A������ƿ����δ�ȹ���ˮ B��δ�������������ȷų����ռ��� C��δ���װ��������
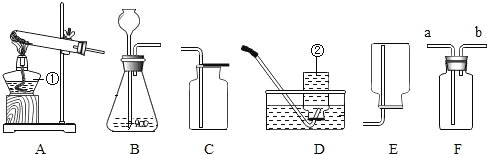
��4��ʵ������ȡ������̼��ԭ����________��_________��ѡ�÷���װ����______������ĸ����д���÷�Ӧ�����ֻ���ű���ʽ __________�������Fװ�����ռ����������̼������Ӧ�ô� ________���c����d��������ͨ�룬��֤�������Ѿ��ռ����ķ���Ϊ___________ ��
��5��ʵ���ҳ���ͼGװ�ô���װ��A��ȡ���壬��װ�õ��ŵ���____________ �����з�Ӧ�����ڸ�װ�õ���_________________������ţ���
��̼���Ʒ�ĩ��ϡ���� ��п����ϡ���� �۹���������Һ���������
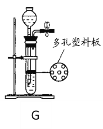
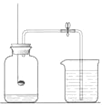
��6����ͼװ�ÿ�������ȡ������̼������������̼�������ʵ���У�������̼���������ͨ��_________��������������Һ����������ʾ��װ����ֲ���͵�������__________������ƿ��δװ��ˮ��Һ���ϵĿ�����ʵ��_______����С����ޡ���Ӱ�졣��������ѹ���¶ȵ�Ӱ�죬�ô���װ�õIJ��������Ȼƫ����ԭ����_______________��
���𰸡�����©���ƾ����Թܿڷ�����ֹ������ؽ��뵼�ܣ��������ܸ������![]() �����+��������+������KMNO4
�����+��������+������KMNO4![]() K2MNO4+MnO2+O2B��CA��B����ʯ��ʯ��ʯ��д��̼��Ʋ����֣�ϡ����A̼���+ϡ������Ȼ���+������̼+ˮ��CaCO3+HCl��CaCl2+CO2+H2Oc��ȼ�ŵ�ľ������d������Ϩ������������ʱ���Ʒ�Ӧ�ķ�����ֹͣ����Ͳ��ֹ������̼����ˮ�����Һ������Ҳ����������������
K2MNO4+MnO2+O2B��CA��B����ʯ��ʯ��ʯ��д��̼��Ʋ����֣�ϡ����A̼���+ϡ������Ȼ���+������̼+ˮ��CaCO3+HCl��CaCl2+CO2+H2Oc��ȼ�ŵ�ľ������d������Ϩ������������ʱ���Ʒ�Ӧ�ķ�����ֹͣ����Ͳ��ֹ������̼����ˮ�����Һ������Ҳ����������������
��������
��1��a����������Ϊ����©����b����������Ϊ�ƾ��ƣ�
��2���ø��������ȡO2����Ҫ��װ��B���Թܿڷ���һ��������ֹ������ؽ��뵼�ܣ��������ܣ�����������ȷֽ�Ϊ����ء��������̺����������ֱ���ʽΪ�������![]() �����+��������+���������ű���ʽΪKMNO4
�����+��������+���������ű���ʽΪKMNO4![]() K2MNO4+MnO2+O2��A��Ӧ�ȼ��װ�õ������ԣ���ֹ�����ݳ���ѡ����ȷ��B��ʵ��ǰ��Ҫ���ݾƾ��Ƶ�λ�ù̶��Թ�λ�ã�ѡ�����C���Ƚ��������뼯��ƿ��������Թܻᵼ��װ���ڿ������뼯��ƿ�У��������������ѡ�����D������ʱ��Ԥ�ȣ��ټ��м��ȣ���ֹ�Թ����Ȳ���������ը�ѣ�ѡ����ȷ���ʱ���ѡBC��
K2MNO4+MnO2+O2��A��Ӧ�ȼ��װ�õ������ԣ���ֹ�����ݳ���ѡ����ȷ��B��ʵ��ǰ��Ҫ���ݾƾ��Ƶ�λ�ù̶��Թ�λ�ã�ѡ�����C���Ƚ��������뼯��ƿ��������Թܻᵼ��װ���ڿ������뼯��ƿ�У��������������ѡ�����D������ʱ��Ԥ�ȣ��ټ��м��ȣ���ֹ�Թ����Ȳ���������ը�ѣ�ѡ����ȷ���ʱ���ѡBC��
��3��A������ƿ����δ�ȹ���ˮ�����¼���ƿ�ڻ��п���������ռ�������������ѡ����ȷ��B��δ�������������ȷų����ռ����ᵼ��װ���ڵĿ���δ�ž��ͽ��뼯��ƿ���������������ѡ����ȷ��C��δ���װ�������ԣ�����ɿ����ռ��������������ռ������ٶȱ�����ѡ����ʱ���ѡAB��
��4��ʵ������ȡ������̼��ԭ���Ǵ���ʯ��ʯ��ʯ��ϡ����÷�Ӧ�ķ�Ӧ�ﳣ���½Ӵ����ɷ�Ӧ���ʲ���Ҫ���ȣ���Ӧװ��ѡA�����ֱ���ʽΪ̼���+ϡ������Ȼ���+������̼+ˮ�����ű���ʽΪCaCO3+HCl��CaCl2+CO2+H2O��������̼�ܶȴ��ڿ���������Fװ�����ռ����������̼������Ӧ�ô�c����ͨ�룻��֤������̼�����ķ���Ϊ��ȼ�ŵ�ľ�����ڼ���ƿ�ڣ�������Ϩ�𣬱�ʾ������
��5��Gװ�ô���װ��A��ȡ���壬���ŵ�Ϊ����ʱ���Ʒ�Ӧ�ķ�����ֹͣ����װ���ʺϹ�����Һ���в���Ӧ��ʵ�飻A��̼����������ϡ���ᣬ�����п��ƣ�ѡ�����B����װ���ʺ�п����ϡ����ķ�Ӧ��ѡ����ȷ��C�����������ڲ��Ӵ��������̵�������Ҳ�����ֽⷴӦ��ѡ����ʱ���ѡ�ڣ�
��6��������̼���������ͨ����Ͳ��Һ����������ʾ��������̼�����Ϊˮ�������ֲ���͵������Ƿ�ֹ������̼����ˮ������ƿ��δװ��ˮ��Һ���ϵĿ�����ʵ��û��Ӱ�죻��������ѹ���¶ȵ�Ӱ�죬�ô���װ�õIJ��������Ȼƫ����ԭ���Ǽ����Һ������Ҳ������������������

����Ŀ��ijͬѧ����±���ʾʵ�飬̽������ͭ�Թ�������ֽ����ʵ�Ӱ�졣
���� | װ�� | ���� |
1.ȡһ��ͭ˿��������Ͳ�Σ��̶�����˿�� |
| |
2.�ֱ���ٺ͢���ע��15 mL��30%�Ĺ���������Һ��������ʢ����ˮ�Ģ��� |
| Լ1 min��ɹ۲쵽�ٺ͢��ж����������ݲ��� |
3.��ͭ˿��������� |
| �����д������ݲ�����5 min���������ݲ�������ʱ������Ȼ���������ݲ��� |
�ش��������⣺
��1���ڲ���3�������ڵ�ʵ��Ŀ����____________��
��2���Ƿ���Եó�ͭ���Լӿ��������ֽ������____________ (ѡ��ǡ���)��
��3�����������ʵ��̽��ͭ�Dz��ǹ�������ֽ�Ĵ�������Ҫ������ʵ�鷽�����в��䣬���б�Ҫ����____________��(�����)
A.����˿����ͭ˿
B.������������������
C.������������Һ��ˮϡ��
D.����ͭ�Ļ�ѧ�����Ƿ����仯
E.����ʵ��ǰͭ˿����������ʵ������ͭ˿��������