题目内容
【题目】同学们用如图所示仪器和装置探究制取气体的方法。请回答下列问题:
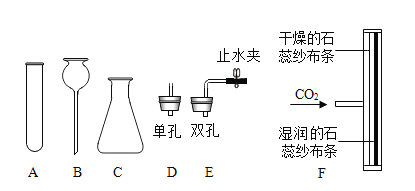
(1)图中仪器B的名称为_____。
(2)组装高锰酸钾制备O2的发生装置,图中还缺少的玻璃仪器是_____(填仪器名称)。
(3)实验室要制取较多量的二氧化碳时,其发生装置的仪器组合为_____(填序号)。
(4)小明利用T形三通管(如图F)设计了探究二氧化碳性质的实验。在通入二氧化碳气体后,观察到的实验现象是_____。
【答案】长颈漏斗 酒精灯 BCE 湿润的石蕊纱布条变红,干燥的石蕊纱布条不变红
【解析】
(1)图中仪器B的名称为长颈漏斗。
(2)组装高锰酸钾制备O2的发生装置,是固体加热型反应,故图中还缺少的玻璃仪器是酒精灯。
(3)实验室要制取较多量的二氧化碳时,需使用较大容器锥形瓶且借助长颈漏斗,故其发生装置的仪器组合为BCE。
(4)利用T形三通管设计探究二氧化碳性质的实验,在通入二氧化碳气体后,由于二氧化碳能与水反应生成碳酸,碳酸能使紫色石蕊变红,故观察到的实验现象是湿润的石蕊纱布条变红,干燥的石蕊纱布条不变红。

 同步练习强化拓展系列答案
同步练习强化拓展系列答案【题目】(1)在化学课上,甲同学将燃烧的钠迅速伸人到盛有CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质。
[提出问题]黑色颗粒和白色物质是什么?
[进行猜想]甲认为黑色颗粒是碳,白色物质可能是Na2O或Na2O和Na2CO3或____________________,乙同学还认为白色物质是氢氧化钠。
甲同学立刻认为乙同学的猜想是错误的,其理由是____________________________________。
[查阅资料]氧化钠为白色粉末,溶于水生成氢氧化钠: ![]() ;常温下饱和Na2CO3溶液的PH值约为12。
;常温下饱和Na2CO3溶液的PH值约为12。
[实验探究]甲同学对白色物质进行实验探究。
实验方案 | 实验操作 | 实验现象 | 结论 |
方案1 | 取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质为Na2O |
方案2 | ① 取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2 溶液 | 出现白色沉淀 | 白色物质是Na2CO3 |
② 静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
[反思评价]丙同学认为方案1得到的结论不正确,其理由是___________________________。
[得出结论]钠在二氧化碳中燃烧的化学方程式为__________________________。
(2)某研究性学习小组设计了用沉淀法测定纯碱( Na2CO3)样品(只含NaCl杂质)中Na2CO3质量分数的实验方案
[实验原理]利用碳酸根离子与钙离子结合生成沉淀,通过沉淀的质量而得出碳酸钠的质量分数
[实验步骤]
①托盘天平称取样品22.0g放人烧杯中,加水使其完全溶解
②验证Na2CO3已完全反应的方法是:静置,向上层清液中滴加____________溶液,如果没有白色沉淀生成,即可证明;
③过滤、操作X、干燥、称量沉淀的质量为20.0g,操作X的名称是___________,如果缺少此操作会造成碳酸钠质量分数___________(填“偏高”“偏低”或“不变”)。
④通过以上提供的数据计算出样品中碳酸钠的质量分数为多少?_____
【题目】小英同学为了测定某地区石灰石样品中碳酸钙的质量分数,取该样品15g,现将75mL的稀盐酸分三次加入石灰石样品中,每次充分反应后测得生成气体的质量,实验数据如下表:
实验 | 第一次 | 第二次 | 第三次 |
加入稀盐酸的量/mL | 25 | 25 | 25 |
生成气体的质量/g | 2.2 | m | 1.1 |
试求:
(1)m的值是 g.
(2)求该样品中碳酸钙的质量分数(保留一位小数).
【题目】实验室常用氯酸钾分解制取氧气。某兴趣小组同学利用下图装置进行实验室制取氧气的实验,待导管口不再有气泡冒出时停止加热,测得相关数据如下表:
试管 | 氯酸钾 | 二氧化锰 | |
实验前质量/g | 18.0 | 14.0 | |
实验后质量/g | 27.2 | ||

(1)证明该装置气密性良好的操作和现象为___________________。
(2)氧气收集完毕后,实验结束的操作步骤是___________________。
(3)固体二氧化锰的作用是___________________,氯酸钾中氯元素的化合价为___________________。
(4)计算实验中加入的二氧化锰的质量______________。
(5)实验室还常用5%的过氧化氢溶液催化分解的方法快速制取氧气。将20%的过氧化氢溶液稀释到5%,所取用的20%的过氧化氢溶液与水的质量比为___________________。