题目内容
【题目】根据如图装置,结合所学化学知识回答下列问题:
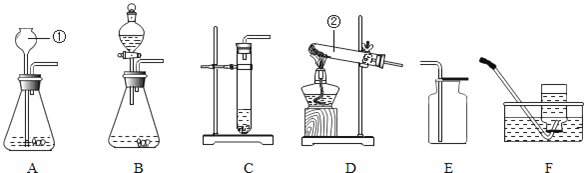
(1)实验室制取少量二氧化碳时,发生装置最好选用 (填字母,下同),收集装置选用 ,只能用此收集方法的原因是 ,如需随时控制反应速率并节约药品,发生装置最好选用 ;
(2)实验室用高锰酸钾制取氧气时,发生装置应选用 (填字母);其反应的化学方程式为 .
(3)如果改用氯酸钾和二氧化锰制取氧气,反应前后二氧化锰的质量分数 (填“增大”、“减小”或“不变”)
【答案】(1)A,E,二氧化碳能溶于水,密度比空气大,B;
(2)D,2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(3)增大.
【解析】
试题分析:(1)根据实验室中制取二氧化碳的反应原理和反应条件来选择反应的发生装置,根据二氧化碳的密度及水溶性来选择收集装置;
(2)据实验室用高锰酸钾制取氧气的原理解答;
(3)催化剂是指能改变其它物质的化学反应速率,而本身的质量和化学性质在化学反应前后都没有改变的物质;因为二氧化锰的质量不变,但是氯酸钾的质量变小,生成了氯化钾和氧气,反应后固体的总质量变小,因此反应前后二氧化锰在固体混合物中的质量分数变大.
解:(1)实验室制取少量二氧化碳可用固液在常温下来制取,故选发生装置C;因为二氧化碳能溶于水,且密度比空气大,所以只能用向上排空气来收集;如需随时控制反应速率并节约药品,发生装置最好选用装置B;
(2)实验室用高锰酸钾制取氧气时,需加热,发生装置应选用D;反应的方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(3)因为二氧化锰的质量不变,但是氯酸钾的质量变小,生成了氯化钾和氧气,反应后固体的总质量变小,因此反应前后二氧化锰在固体混合物中的质量分数变大.
故答案为:(1)A,E,二氧化碳能溶于水,密度比空气大,B;
(2)D,2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(3)增大.