题目内容
35、为了测定水的组成选用下列装置回答问题:(氢气用盐酸和锌制得)
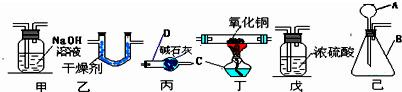
(1)为准确测定水的组成,为防止杂质干扰,正确的连接顺序为:己→
(2)乙装置的作用是
(3)若测得丁装置中样品在实验前后减少6.4克,乙装置中药品增加了7.2克,丙装置增加了3.6克,根据此可求出水中H、O质量比为(只写计算式)
(4)实验结束后,若丁处仍有黑色固体,这对实验的结果的影响是
(5)装置中的丙能否省去?
为什么?

(1)为准确测定水的组成,为防止杂质干扰,正确的连接顺序为:己→
甲→戊→丁→乙
→丙;(2)乙装置的作用是
吸收氢气还原氧化铜后生成的水
.(3)若测得丁装置中样品在实验前后减少6.4克,乙装置中药品增加了7.2克,丙装置增加了3.6克,根据此可求出水中H、O质量比为(只写计算式)
(7.2-6.4):6.4
.(4)实验结束后,若丁处仍有黑色固体,这对实验的结果的影响是
无影响
(填“氧的质量偏大”、“氢的质量偏大”、“无影响”);(5)装置中的丙能否省去?
不能
为什么?
它的目的是吸收空气中的水蒸气,否则会影响实验的结果
.分析:测定水的组成的实验思路为:
利用金属与酸反应产生的氢气还原金属氧化物,测定丁中金属氧化物和乙中干燥剂反应前后的质量.丁中金属氧化物反应前后的质量减少,减少的质量就是金属氧化物中失去的氧元素的质量,即生成的水中氧元素的质量;乙中干燥剂反应前后质量增重,增重的质量即为生成的水的质量.
利用金属与酸反应产生的氢气还原金属氧化物,测定丁中金属氧化物和乙中干燥剂反应前后的质量.丁中金属氧化物反应前后的质量减少,减少的质量就是金属氧化物中失去的氧元素的质量,即生成的水中氧元素的质量;乙中干燥剂反应前后质量增重,增重的质量即为生成的水的质量.
解答:解:(1)为准确测定水的组成,为防止杂质干扰,正确的连接顺序为:己→甲→戊→丁→乙→丙.从己中生成的氢气带有氯化氢气体和水蒸气,依次通过甲和戊除去,然后再通过丁还原氧化铜,反应后生成的水蒸气经过乙被吸收,最后再连接丙装置,丙的作用是吸收空气中的水蒸气,以免进入乙装置影响测定结果.实验结束后,若丁处仍有黑色固体,这对实验的结果无影响,因为实验中需要的数据是金属氧化物反应前后减少的质量,即为水中氧元素的质量.
(2)丁中金属氧化物反应前后减少的质量为6.4克,即水中氧元素的质量;乙装置增加的质量7.2克即为生成水的质量;7.2克-6.4克为氢元素的质量.根据此可求出水中H、O质量比为(7.2-6.4):6.4.
故答案是:(1)甲→戊→丁→乙;
(2)吸收氢气还原氧化铜后生成的水;
(3)无影响;
(4)不能;它的目的是吸收空气中的水蒸气,否则会影响实验的结果.
(2)丁中金属氧化物反应前后减少的质量为6.4克,即水中氧元素的质量;乙装置增加的质量7.2克即为生成水的质量;7.2克-6.4克为氢元素的质量.根据此可求出水中H、O质量比为(7.2-6.4):6.4.
故答案是:(1)甲→戊→丁→乙;
(2)吸收氢气还原氧化铜后生成的水;
(3)无影响;
(4)不能;它的目的是吸收空气中的水蒸气,否则会影响实验的结果.
点评:此题考查测定水的组成的综合实验,有利于培养学生对化学知识的综合运用能力.解题有以下要点:1、一套完整的实验装置应由以下四个部分组成:发生装置+净化装置+性质实验装置+尾气处理装置;2、净化气体时:一般除杂在先,干燥在后.测定水的组成需要确切的实验数据,因此在实验装置的选择中,要尽量消除各种对实验数据和结果的干扰因素.

练习册系列答案
相关题目




 为了测定水的组成选用下列装置回答问题:(提示:1、氢气用盐酸和锌制得2、实验原理:利用纯净的氢气还原氧化铜测定生成水的质量,从而确定H、O的质量.)
为了测定水的组成选用下列装置回答问题:(提示:1、氢气用盐酸和锌制得2、实验原理:利用纯净的氢气还原氧化铜测定生成水的质量,从而确定H、O的质量.)