题目内容
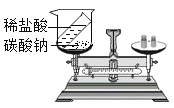
【题目】为测定某矿山开采的石灰石样品中碳酸钙的质量分数,进行下列操作:取6g石灰石样品,将其敲碎后,放入烧杯内(烧杯质量为20g),再加入50g足量的稀盐酸使其完全反应(杂质不与盐酸反应)。反应所需时间(t)和烧杯及其所盛物质总重量(m)的关系如图所示,试计算:
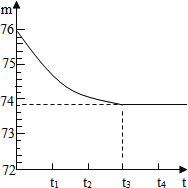
(1)实验结束时共放出二氧化碳______g;
(2)该石灰石样品中碳酸钙的质量分数________(计算结果保留小数点一位)
【答案】2.2 83.3%
【解析】
解:(1)图中质量轴上每个小刻度表示0.2g,所以完全放出气体后剩余物质总质量为73.8g;
根据质量守恒定律,反应前后物质的总质量不变,因此放出气体二氧化碳的质量=76g-73.8g=2.2g;
(2)设石灰石样品中碳酸钙的质量为x

![]()
x=5g
该石灰石样品中碳酸钙的质量分数为:![]() ×100%=83.3%,
×100%=83.3%,
答:该石灰石样品中碳酸钙的质量分数是83.3%。

 名校课堂系列答案
名校课堂系列答案【题目】(4分)KNO3和KCl在不同温度时的溶解度如下表所示。请回答下列问题:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | |
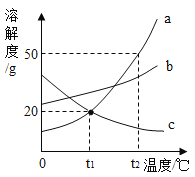
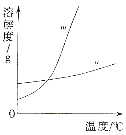
(1)依据上表数据,绘制KNO3和KCl的溶解度曲线,右图中能表示KNO3溶解度曲线的是 。(填m或n)
(2)由表中数据分析可知, KNO3和KCl在某一温度时具有相同的溶解度x,则x的取值范围是 。
(3)10℃时,131g 饱和KCl溶液,蒸发10g水后,再降温到10℃,可析出KCl晶体的质量为 。
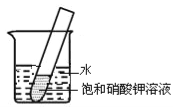
(4)如右图所示,20℃时,将盛有饱和KNO3溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出。加入的物质可能是下列中的________(填字母序号)。
A.氢氧化钠固体 B.生石灰固体
C.冰块 D.硝酸铵固体
E.浓硫酸
【题目】KNO3和KCl在不同温度时的溶解度如表所示.请回答下列问题:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
溶解度 | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 |
(1)由表中数据分析可知,KNO3和KCl在某一温度时具有相同的溶解度x,则x的取值范围是______.
(2)10℃时,131g饱和KCl溶液,蒸发10g水后,再降温到10℃,可析出KCl晶体的质量为______.
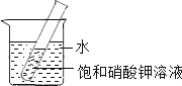
(3)如图所示,20℃时,将盛有饱和KNO3溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出.加入的物质可能是下列中的______(填字母序号).
a.氢氧化钠固体 b.生石灰固体 c.硝酸铵固体