题目内容
(2013?雅安)废铁屑的主要成份是铁,同时还有少量铁锈(Fe2O3),动物饲料硫酸亚铁的生产工艺之一如下图所示:
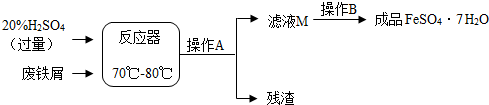
(1)在反应器中发生反应的化学方程式除Fe2(SO4)3+Fe=3FeSO4外还有:
(2)滤液M中肯定含有的溶质的化学式是
(3)在实验室中完成操作A的玻璃仪器有玻璃棒、烧杯和
(4)滤液M经过操作B可得硫酸亚铁晶体(FeSO4?7H2O).已知硫酸亚铁的溶解度和析出晶体的组成如下表:
根据溶解度表,硫酸亚铁晶体(FeSO4?7H2O)冷却结晶温度最高不超过
(5)在化学反应中,若有元素化合价变化的反应定义为氧化还原反应.下列反应类型肯定是氧化还原反应的是
A.化合反应B.置换反应C.分解反应D.复分解反应
在氧化还原反应中,若有元素的化合价升高,必有元素的化合价降低,且元素化合价升降总数相等.
将无水硫酸亚铁(FeSO4)隔绝空气加强热,生成产物有三氧化二铁和其它氧化物,试写出该反应的化学方程式

(1)在反应器中发生反应的化学方程式除Fe2(SO4)3+Fe=3FeSO4外还有:
Fe+H2SO4═FeSO4+H2↑;Fe2O3+3H2SO4═Fe2(SO4)3+3H2O
Fe+H2SO4═FeSO4+H2↑;Fe2O3+3H2SO4═Fe2(SO4)3+3H2O
;(2)滤液M中肯定含有的溶质的化学式是
FeSO4、H2SO4
FeSO4、H2SO4
;(3)在实验室中完成操作A的玻璃仪器有玻璃棒、烧杯和
漏斗
漏斗
;(4)滤液M经过操作B可得硫酸亚铁晶体(FeSO4?7H2O).已知硫酸亚铁的溶解度和析出晶体的组成如下表:
| 温度/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 | |
| 溶解度/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | 37.2 | |
| 析出晶体 | FeSO4?7H2O | FeSO4?4H2O | FeSO4?H2O | ||||||||
64
64
℃;(5)在化学反应中,若有元素化合价变化的反应定义为氧化还原反应.下列反应类型肯定是氧化还原反应的是
B
B
(填字母编号);A.化合反应B.置换反应C.分解反应D.复分解反应
在氧化还原反应中,若有元素的化合价升高,必有元素的化合价降低,且元素化合价升降总数相等.
将无水硫酸亚铁(FeSO4)隔绝空气加强热,生成产物有三氧化二铁和其它氧化物,试写出该反应的化学方程式
2FeSO4
Fe2O3+SO2↑+SO3↑
| ||
2FeSO4
Fe2O3+SO2↑+SO3↑
.
| ||
分析:(1)铁和氧化铁都能和稀硫酸反应,可以据此写出反应的化学方程式;
(2)加入的硫酸是过量的,所以在溶液中含有硫酸和反应生成的硫酸亚铁,可以据此解答该题;
(3)操作a为过滤,所以还需要漏斗,可以据此解答该题;
(4)根据图表中的信息可以知道当问到大于64℃时产生了FeSO4?4H2O,可以据此解答该题;
(5)根据四种基本反应类型的特点来解答该题,根据题给的信息可以判断无水硫酸亚铁(FeSO4)隔绝空气加强热,生成产物有三氧化二铁、二氧化硫和三氧化硫,可以据此写出该反应的化学方程式.
(2)加入的硫酸是过量的,所以在溶液中含有硫酸和反应生成的硫酸亚铁,可以据此解答该题;
(3)操作a为过滤,所以还需要漏斗,可以据此解答该题;
(4)根据图表中的信息可以知道当问到大于64℃时产生了FeSO4?4H2O,可以据此解答该题;
(5)根据四种基本反应类型的特点来解答该题,根据题给的信息可以判断无水硫酸亚铁(FeSO4)隔绝空气加强热,生成产物有三氧化二铁、二氧化硫和三氧化硫,可以据此写出该反应的化学方程式.
解答:解:(1)铁和氧化铁都能和稀硫酸反应生成了硫酸亚铁和氢气,而反应生成了硫酸铁和水,可以据此写出反应的化学方程式;
(2)加入的硫酸是过量的,所以在溶液中含有硫酸和反应生成的硫酸亚铁;
(3)操作a后得到了滤液和固体,所以可以判断操作a为过滤,所以还需要的玻璃仪器为漏斗,;
(4)根据图表中的信息可以知道当问到大于64℃时产生了FeSO4?4H2O,所以应该将温度控制在64℃以下;
(5)根据四种基本反应类型的特点可以知道,在置换反应中有单质参与和生成新的单质,所以可以判断在置换反应中一定有化合价的变化,故选B,根据题给的信息可以判断无水硫酸亚铁(FeSO4)隔绝空气加强热,生成产物有三氧化二铁和三氧化硫,在氧化还原反应中,若有元素的化合价升高,必有元素的化合价降低,且元素化合价升降总数相等,所以结合元素化合价的变化可以知道,铁元素的化合价由+2变成了+3价,所以反应中有二氧化硫生成,硫元素的化合价由+6降低到+4,所以根据质量守恒定律可以判断在该反应中还生成了三氧化硫,所以该反应的化学方程式为:2FeSO4
Fe2O3+SO2↑+SO3↑.
故答案为:(1)Fe+H2SO4═FeSO4+H2↑; Fe2O3+3H2SO4═Fe2(SO4)3+3 H2O;
(2)FeSO4、H2SO4;
(3)漏斗;
(4)64;
(5)B;2FeSO4
Fe2O3+SO2↑+SO3↑.
(2)加入的硫酸是过量的,所以在溶液中含有硫酸和反应生成的硫酸亚铁;
(3)操作a后得到了滤液和固体,所以可以判断操作a为过滤,所以还需要的玻璃仪器为漏斗,;
(4)根据图表中的信息可以知道当问到大于64℃时产生了FeSO4?4H2O,所以应该将温度控制在64℃以下;
(5)根据四种基本反应类型的特点可以知道,在置换反应中有单质参与和生成新的单质,所以可以判断在置换反应中一定有化合价的变化,故选B,根据题给的信息可以判断无水硫酸亚铁(FeSO4)隔绝空气加强热,生成产物有三氧化二铁和三氧化硫,在氧化还原反应中,若有元素的化合价升高,必有元素的化合价降低,且元素化合价升降总数相等,所以结合元素化合价的变化可以知道,铁元素的化合价由+2变成了+3价,所以反应中有二氧化硫生成,硫元素的化合价由+6降低到+4,所以根据质量守恒定律可以判断在该反应中还生成了三氧化硫,所以该反应的化学方程式为:2FeSO4
| ||
故答案为:(1)Fe+H2SO4═FeSO4+H2↑; Fe2O3+3H2SO4═Fe2(SO4)3+3 H2O;
(2)FeSO4、H2SO4;
(3)漏斗;
(4)64;
(5)B;2FeSO4
| ||
点评:掌握化学方程式的书写、盐的化学性质等知识,并学会分析信息、提取信息,并应用所学知识结合所给信息进行解答,考查了学生分析、解决问题的能力.

练习册系列答案
相关题目