题目内容
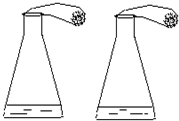 实验室有失去标签的两瓶白色粉末药品,分别是Na2CO3和NaHCO3.某同学设计了下列实验进行鉴别,如图所示.
实验室有失去标签的两瓶白色粉末药品,分别是Na2CO3和NaHCO3.某同学设计了下列实验进行鉴别,如图所示.
| 步骤 | 实验操作 |
| 1 | 往两个相同的锥形瓶中分别加入50g溶质质量分数为14.6%的稀盐酸 |
| 2 | 用相同两只气球,分别装入足量的两瓶中的白色粉末各20g,套在步骤1的锥形瓶口,如图 |
| 3 | 迅速将气球中的药品,倒入锥形瓶中 |
①算两瓶中产生二氧化碳各多少克?
②判断该同学的实验操作能否达到鉴别的目的?并说明理由.
解:(1)稀盐酸中HCl的质量为:50g×14.6%=7.3g
设:碳酸钠和盐酸反应生成二氧化碳的质量为x.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
73 44
7.3g x

x=4.4g
设碳酸氢钠和盐酸反应生成二氧化碳的质量为y.
NaHCO3+HCl=NaCl+H2O+CO2↑
36.5 44
7.3g y
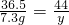
y=8.8g
答:碳酸钠和盐酸反应生成二氧化碳的质量为4.4g,碳酸氢钠和盐酸反应生成二氧化碳的质量为8.8g.
(2)能达到目的.气球大的是碳酸氢钠,气球小的是碳酸钠.
分析:(1)根据由Na2CO3+2HCl=2NaCl+H2O+CO2↑和NaHCO3+HCl=NaCl+H2O+CO2↑可知,Na2CO3和NaHCO3各20g,需要HCl的质量都大于7.3g,所以稀盐酸均不足,所以只能用HCl的质量做为已知量进行计算求出二氧化碳的质量即可;
(2)根据二者生成二氧化碳的质量不同判断出气球的大小从而确定药品的成分.
点评:本题通过不同的实验探究对碳酸钠和碳酸氢钠的化学性质进行了全面的考查,难度较大.
设:碳酸钠和盐酸反应生成二氧化碳的质量为x.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
73 44
7.3g x

x=4.4g
设碳酸氢钠和盐酸反应生成二氧化碳的质量为y.
NaHCO3+HCl=NaCl+H2O+CO2↑
36.5 44
7.3g y
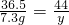
y=8.8g
答:碳酸钠和盐酸反应生成二氧化碳的质量为4.4g,碳酸氢钠和盐酸反应生成二氧化碳的质量为8.8g.
(2)能达到目的.气球大的是碳酸氢钠,气球小的是碳酸钠.
分析:(1)根据由Na2CO3+2HCl=2NaCl+H2O+CO2↑和NaHCO3+HCl=NaCl+H2O+CO2↑可知,Na2CO3和NaHCO3各20g,需要HCl的质量都大于7.3g,所以稀盐酸均不足,所以只能用HCl的质量做为已知量进行计算求出二氧化碳的质量即可;
(2)根据二者生成二氧化碳的质量不同判断出气球的大小从而确定药品的成分.
点评:本题通过不同的实验探究对碳酸钠和碳酸氢钠的化学性质进行了全面的考查,难度较大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
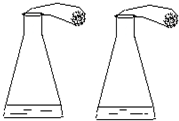 实验室有失去标签的两瓶白色粉末药品,分别是Na2CO3和NaHCO3.某同学设计了下列实验进行鉴别,如图所示.
实验室有失去标签的两瓶白色粉末药品,分别是Na2CO3和NaHCO3.某同学设计了下列实验进行鉴别,如图所示.