题目内容
【题目】物质是由元素组成的,如图为元素周期表的一部分请按要求填空: 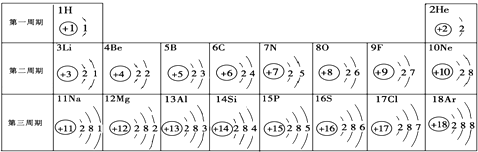
(1)表中3至10号元素位于第二周期,11至18号元素位于第三周期,分析其规律可知,每一周期元素原子的相同.
(2)在元素周期表中,同一族(纵行)的元素具有相似的化学性质则下列各组元素具有相似化学性质的是(填标号).
A.C和Si
B.Al和Mg
C.P和Si
D.F和Cl
(3)表中17号元素在化学反应中易(填“得到”或“失去”)电子,形成的离子符号为 , 若12号和17号元素组成化合物,则化学式为 .
【答案】
(1)电子层数
(2)AD
(3)得到;Cl-;MgCl2
【解析】解:(1)第二周期的3﹣10号元素原子的电子层数相同,第三周期的11﹣18号元素原子的电子层数也相同,因此得出规律每一周期元素原子的电子层数相同;所以答案是:电子层数;(2)根据题意,同一族(纵行)的元素具有相似的化学性质,C和Si、F和Cl属于同一族(纵行),化学性质相似.故填:AD;(3)17号元素是氯元素,其最外层有7个电子,在化学反应中易得到1个电子而形成带一个单位负电荷的氯离子,在化合物中常显﹣1价,12号元素是镁元素,在化合物中常显+2价,二者组成的化合物的化学式为MgCl2;故填:得到;Cl-;MgCl2 .

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目