题目内容
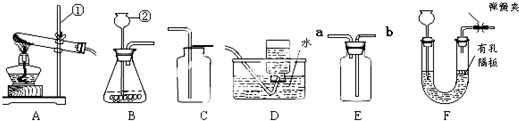
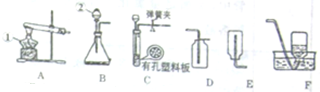
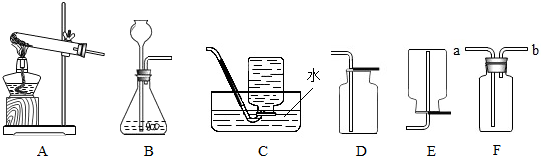
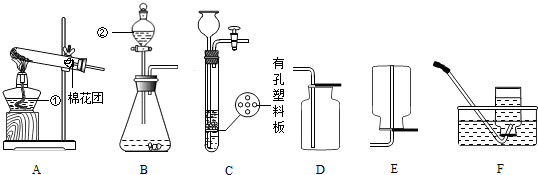
结合图回答问题:
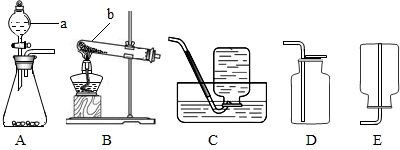
(1)写出图中标号的仪器名称:a
(2)有多种途径可以产生氧气.如:A.分离空气 B.加热高锰酸钾 C.分解过氧化氢
相信你在D处还可以写出另一种能产生氧气的方法 D.
(3)写出实验室用A装置制取氧气的符号表达式
(4)若用加热高锰酸钾制取氧气,选用的发生装置是
(5)若用B、C组合来制取某种气体,应满足下列条件中的
①反应物都是固体 ②反应需要加热 ③制得的气体不易溶于水 ④气体密度比水大
A.①②③④B.①②C.②④D.①②③

(1)写出图中标号的仪器名称:a
分液漏斗
分液漏斗
;b试管
试管
.(2)有多种途径可以产生氧气.如:A.分离空气 B.加热高锰酸钾 C.分解过氧化氢
相信你在D处还可以写出另一种能产生氧气的方法 D.
加热氯酸钾(或电解水)
加热氯酸钾(或电解水)
(3)写出实验室用A装置制取氧气的符号表达式
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.
| ||
(4)若用加热高锰酸钾制取氧气,选用的发生装置是
B
B
,若要收集较干燥的氧气应选D
D
;若要收集较纯净的氧气可选C
C
收集装置; 实验结束,停止加热要先把导管移出水面,其理由是若先移去酒精灯,会造成冷水倒流,试管炸裂
若先移去酒精灯,会造成冷水倒流,试管炸裂
;此时发现水槽中的水变成了浅紫红色,你认为产生该现象的原因可能是试管口没有放一团棉花
试管口没有放一团棉花
;(5)若用B、C组合来制取某种气体,应满足下列条件中的
D
D
①反应物都是固体 ②反应需要加热 ③制得的气体不易溶于水 ④气体密度比水大
A.①②③④B.①②C.②④D.①②③
分析:(1)识别一些简单仪器;
(2)实验室通常用分解过氧化氢溶液、加热氯酸钾、加热高锰酸钾的方法制取氧气,电解水也可生成氧气;
(3)A装置适用于固体和液体不需加热制取气体,过氧化氢溶液分解制取氧气可用此装置,据此书写方程式;
(4)根据高锰酸钾制取氧气的反应物的状态和反应条件选择发生装置,收集干燥的氧气用排空气法,收集较纯净的气体用排水法;并据实验注意事项回答;
(5)B装置适用于加热固体制取气体,排水法收集不溶于水或不易溶于水的气体.
(2)实验室通常用分解过氧化氢溶液、加热氯酸钾、加热高锰酸钾的方法制取氧气,电解水也可生成氧气;
(3)A装置适用于固体和液体不需加热制取气体,过氧化氢溶液分解制取氧气可用此装置,据此书写方程式;
(4)根据高锰酸钾制取氧气的反应物的状态和反应条件选择发生装置,收集干燥的氧气用排空气法,收集较纯净的气体用排水法;并据实验注意事项回答;
(5)B装置适用于加热固体制取气体,排水法收集不溶于水或不易溶于水的气体.
解答:解:(1)标号仪器分别是分液漏斗和试管;
(2)根据实验室制氧气的三种方法可知:还可用加热氯酸钾的方法制取氧气,此外,电解水也能生成氧气;
(3)A装置适用于固体和液体不需加热制取气体,过氧化氢溶液分解制取氧气可用此装置,过氧化氢在二氧化锰催化作用下分解生成水和氧气;
(4)加热高锰酸钾制取氧气,属于固体加热型,故选发生装置B;氧气的密度比空气大且不易溶于水,故要收集较干燥的氧气应用向上排空气法,要收集较纯净的氧气用排水法;实验结束,停止加热要先把导管移出水面,防止试管温度降低,压强减小,水倒吸入试管引起试管炸裂;水槽中的水变成红色是因为:试管口没有塞一团棉花,加热时高锰酸钾粉末飞溅进入了水槽;
(5)根据BC装置特点,若用B、C组合来制取某种气体,则须满足:反应物都是固体,反应需要加热,制得的气体不易溶于水;
故答案为:(1)分液漏斗;试管;
(2)加热氯酸钾(或电解水);
(3)2H2O2
2H2O+O2↑;
(4)B;D;C;若先移去酒精灯,会造成冷水倒流,试管炸裂;试管口没有放一团棉花;
(5)D.
(2)根据实验室制氧气的三种方法可知:还可用加热氯酸钾的方法制取氧气,此外,电解水也能生成氧气;
(3)A装置适用于固体和液体不需加热制取气体,过氧化氢溶液分解制取氧气可用此装置,过氧化氢在二氧化锰催化作用下分解生成水和氧气;
(4)加热高锰酸钾制取氧气,属于固体加热型,故选发生装置B;氧气的密度比空气大且不易溶于水,故要收集较干燥的氧气应用向上排空气法,要收集较纯净的氧气用排水法;实验结束,停止加热要先把导管移出水面,防止试管温度降低,压强减小,水倒吸入试管引起试管炸裂;水槽中的水变成红色是因为:试管口没有塞一团棉花,加热时高锰酸钾粉末飞溅进入了水槽;
(5)根据BC装置特点,若用B、C组合来制取某种气体,则须满足:反应物都是固体,反应需要加热,制得的气体不易溶于水;
故答案为:(1)分液漏斗;试管;
(2)加热氯酸钾(或电解水);
(3)2H2O2
| ||
(4)B;D;C;若先移去酒精灯,会造成冷水倒流,试管炸裂;试管口没有放一团棉花;
(5)D.
点评:本题考查学生根据实验室制取氧气,二氧化碳的反应原理,装置,收集的方法和操作注意事项进行分析解题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目