题目内容
【题目】如图为四种物质的溶解度曲线,则下列说法错误的是( ) 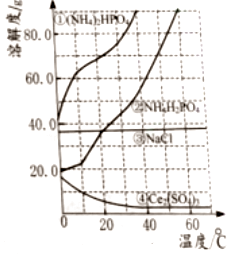
A.当温度为10℃时,物质溶解度关系为①>③>②>④
B.若NH4H2PO4中混有少量NaCl杂质,可在较高温度配成饱和溶液,再降温结晶
C.在10℃时把NH4H2PO4和Ce2(SO4)3的饱和溶液升温到30℃,有晶体析出的是Ce2(SO4)3
D.22℃时(NH4)2HPO4饱和溶液的质量分数约为70%
【答案】D
【解析】解:A、通过分析溶解度曲线可知,当温度为10℃时,物质溶解度关系为①>③>②>④,故A正确; B、磷酸二氢铵的溶解度受温度变化影响较大,所以NH4H2PO4中混有少量NaCl杂质,可在较高温度配成饱和溶液,再降温结晶,故B正确;
C、Ce2(SO4)3的溶解度随温度的升高而减小,所以在10℃时把NH4H2PO4和Ce2(SO4)3的饱和溶液升温到30℃,有晶体析出的是Ce2(SO4)3 , 故C正确;
D、22℃时,磷酸氢二铵的溶解度是70g,所以(NH4)2HPO4饱和溶液的质量分数约为: ![]() ×100%=41.2%,故D错误.
×100%=41.2%,故D错误.
故选:D.
【考点精析】利用结晶的原理、方法及其应用和固体溶解度曲线及其作用对题目进行判断即可得到答案,需要熟知结晶的两种方法:蒸发溶剂,如NaCl(海水晒盐)和降低温度(冷却热的饱和溶液,如KNO3);1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性.2.比较相同温度时(或一定温度范围内)不同物质溶解度的大小.3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法.4.确定溶液的状态(饱和与不饱和).

【题目】某合金与铁的物理性质比较如下表所示:
物理性质 | 熔点 | 密度 | 硬度 | 导电性 |
某合金 | 3 200 ℃ | 3.20 g·cm-3 | 7.5 | 3.5 |
铁 | 1 535 ℃ | 7.86 g·cm-3 | 4.5 | 17 |
(注:硬度以金刚石的硬度为10作标准,导电性以银的导电性为100作标准)
已知该合金耐腐蚀、强度大,从性能上看,该合金不适合制(_________)
A. 门窗框 B. 炊具 C. 导线 D. 航天器