题目内容
(5分)物质都是由粒子构成的,化学反应的实质是粒子之间的重新组合。
(1)右图为甲、乙两种不同的气态物质在一定条件下反应生成丙物质的微观示意图,其中 和
和 分别表示氢原子和氮原子,则可知:
分别表示氢原子和氮原子,则可知:
①一个丙分子由 个原子构成。
②构成甲物质的粒子是 (填“分子”、“原子”或“离子”)。
③此反应中甲、乙、丙三种物质的粒子个数比为 。
(2)把一定质量的纯净物A和80 g B在一定条件下按下图所示充分反应,当B消耗完时,可生成88 g D物质和18 g E物质。
请回答下列问题:
①参加反应的A物质的质量是 。
②A分子中各元素的原子个数比是(需表示出元素种类) 。
(1)① 4 ②分子 ③ 3∶1∶2
(2)① 26 g ②C∶H=1∶1
解析试题分析:(1)①根据微观示意图,可看出一个丙分子由4个原子构成;
②由微观示意图可知,构成甲物质的粒子是由2个氢原子构成的氢分子;
③根据微观示意图和质量守恒定律,写出反应的化学方程式:3H2+N2=2NH3,则此反应中甲、乙、丙三种物质的粒子个数比为3:1:2;
(2)①根据质量守恒定律,A物质的质量=D物质质量+E物质质量-B物质质量=88g+18g-80g=26g;
②根据微观示意图可知,B为氧气,D为二氧化碳,E为水;再根据质量守恒定律中,元素种类、质量都不变,可知:
A物质中C元素的质量为:88g×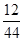 =24g;
=24g;
A物质中H元素的质量为:18g×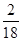 =2g;
=2g;
则A物质中O元素的质量为:26g-24g-2g=0,
故A物质中只有C、H两种元素,且C的质量:H的质量=24g:2g=12:1,
设A的化学式为CxHy,则有12x:y=12:1,故C的个数:H的个数=1:1。
考点:质量守恒定律及其应用
点评:解答这类题,首先要能理解微粒示意图所提供的信息,并能根据微粒示意图分析问题;另外,理解和掌握质量守恒定律是解答本题的关键。

 全能测控一本好卷系列答案
全能测控一本好卷系列答案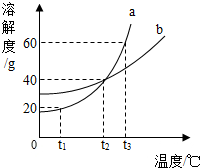 (1)某原子结构示意图为
(1)某原子结构示意图为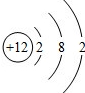 该原子核内有
该原子核内有(2)世界上的物质都是由粒子构成的,仿照示例填空
| 物质名称 | 示例:水 | 铁 | 氯化钠 | |
| 构成物质的粒子 | 分子 | 分子 |
根据该图可知:在t3℃时,a物质的溶解度是


