题目内容
根据表中内容回答下列问题.
(1)随温度升高,硝酸钾溶解度的变化趋势是________(填“增大”“减小”或“不变”).
(2)根据上表推断硝酸钾与氯化钠溶解度相等时的温度范围是________.
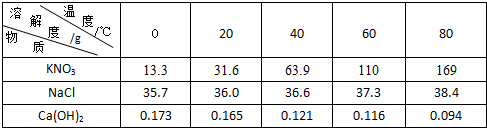
(3)取KNO3、NaCl两种固体各36g分别放入20℃时的100g水中充分溶解,20℃时有如图1所示的实验现象,烧杯b中溶解的物质________.
(4)如图2所示,若向烧杯中加入足量的硝酸铵使之充分溶解,可观察到的现象是________.
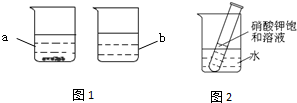 (5)如图2所示,若向试管中加入少量的硝酸钾固体,再向烧杯中加入足量的生石灰,可观察到的现象是________.
(5)如图2所示,若向试管中加入少量的硝酸钾固体,再向烧杯中加入足量的生石灰,可观察到的现象是________.
解:(1)分析表格数据,硝酸钾的溶解度随温度的升高而升高.
(2)硝酸钾和氯化钠溶解度相同的温度既是判断该段中溶解度的数值是否存在相等的可能,经分析知在20~40℃时这两种物质存在溶解度相同的可能.
(3)由表格数据可得出20℃时100g水中最多可溶解硝酸钾31.6g,可溶解氯化钠36g,所以题中向100g水中加入36g溶质,氯化钠刚好得到饱和,硝酸钾不会全部溶解.
(4)硝酸铵溶解吸收热量温度降低;硝酸钾的溶解度随温度的降低溶解度减小;故可观察到烧杯内水温下降,试管中有晶体析出;
(5)生石灰与水反应放出热量温度升高,硝酸钾的溶解度随温度的升高溶解度增大;故可观察到烧杯内浑浊,水温上升,试管内固体逐渐溶解.
故答案为(1)增大.
(2)20~40℃.
(3)NaCl.
(4)烧杯内水温下降,试管中有晶体析出;
(5)烧杯内浑浊,水温上升,试管内固体逐渐溶解.
分析:(1)分析表中数据总结硝酸钾溶解度随温度变化规律即可.
(2)硝酸钾和氯化钠溶解度相同的温度即是判断该段中溶解度的数值是否存在相等的可能.
(3)通过表格的溶解度来判断.
(4)硝酸铵溶解吸收热量温度降低;硝酸钾的溶解度随温度的降低溶解度减小;
(5)生石灰与水反应放出热量温度升高,硝酸钾的溶解度随温度的升高溶解度增大;
点评:溶解度是溶液部分的重难点,也是历年中考热点之一,学习中要透彻理解溶解度的有关知识.
(2)硝酸钾和氯化钠溶解度相同的温度既是判断该段中溶解度的数值是否存在相等的可能,经分析知在20~40℃时这两种物质存在溶解度相同的可能.
(3)由表格数据可得出20℃时100g水中最多可溶解硝酸钾31.6g,可溶解氯化钠36g,所以题中向100g水中加入36g溶质,氯化钠刚好得到饱和,硝酸钾不会全部溶解.
(4)硝酸铵溶解吸收热量温度降低;硝酸钾的溶解度随温度的降低溶解度减小;故可观察到烧杯内水温下降,试管中有晶体析出;
(5)生石灰与水反应放出热量温度升高,硝酸钾的溶解度随温度的升高溶解度增大;故可观察到烧杯内浑浊,水温上升,试管内固体逐渐溶解.
故答案为(1)增大.
(2)20~40℃.
(3)NaCl.
(4)烧杯内水温下降,试管中有晶体析出;
(5)烧杯内浑浊,水温上升,试管内固体逐渐溶解.
分析:(1)分析表中数据总结硝酸钾溶解度随温度变化规律即可.
(2)硝酸钾和氯化钠溶解度相同的温度即是判断该段中溶解度的数值是否存在相等的可能.
(3)通过表格的溶解度来判断.
(4)硝酸铵溶解吸收热量温度降低;硝酸钾的溶解度随温度的降低溶解度减小;
(5)生石灰与水反应放出热量温度升高,硝酸钾的溶解度随温度的升高溶解度增大;
点评:溶解度是溶液部分的重难点,也是历年中考热点之一,学习中要透彻理解溶解度的有关知识.

练习册系列答案
相关题目



 (5)如图2所示,若向试管中加入少量的硝酸钾固体,再向烧杯中加入足量的生石灰,可观察到的现象是
(5)如图2所示,若向试管中加入少量的硝酸钾固体,再向烧杯中加入足量的生石灰,可观察到的现象是
 采取的方法有
采取的方法有 象,烧杯b中溶解的物质是
象,烧杯b中溶解的物质是