题目内容
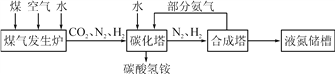
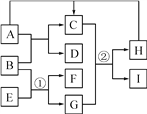
【题目】已知A~I均为初中化学常见的物质,其中组成A、C两种气体的元素相同,且C是常见的温室气体,B是铁锈的主要成分,D是单质,F是盐酸盐,根据如图所示的转化关系(图中反应条件均已略去)回答下列问题:
(1)D的化学式为____。
(2)写出反应①的化学方程式____。
(3)若反应②在植物体内进行,这个过程中能量的转化形式是____。
【答案】(1)Fe (2)Fe2O3+6HCl═2FeCl3+3H2O;(3)光能转化为化学能
【解析】试题分析:由题意,组成A、C两种气体的元素相同,且C是常见的温室气体,则C为二氧化碳,则A为一氧化碳;B是铁锈的主要成分,则B为氧化铁,一氧化碳与氧化铁在高温下反应生成铁和二氧化碳,则D为铁;氧化铁与E反应生成的F是盐酸盐,结合金属氧化物能与酸反应,则E为稀盐酸,G为水;二氧化碳与水发生光合作用生成葡萄糖和氧气,故(1)D的化学式为Fe.
(2)反应①,即氧化铁与稀盐酸反应生成氯化铁和水,反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O. (3)反应②在植物体内进行,即二氧化碳与水发生光合作用生成葡萄糖和氧气,这个过程中能量的转化形式光能转化为化学能.

 初中学业考试导与练系列答案
初中学业考试导与练系列答案【题目】以下是老师引导学生探究“质量守恒定律”的教学片段,请你参与探究并帮忙填写空格(包括表中的空格)。
【提出问题】 化学反应前后各物质的质量总和是否相等?
【查阅资料】 氢氧化钠溶液可以吸收二氧化碳气体
【猜想与假设】 猜想1:不相等;猜想2:相等。
【实验探究】 甲、乙两组同学用托盘天平分别称量反应前后物质的质量。
甲组 | 乙组 | |
实验方案(反应后略) |
|
|
实验现象 | 有气泡产生,天平指针向右偏转 | _________,天平指针没有偏转 |
结论 | 猜想1正确,反应的化学方程 式:_______________. | 猜想2正确 |
【反思评价】 究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体溢出,导致指针向右偏转。得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加的反应一定要在_______________中进行。
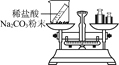
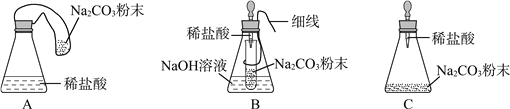
【优化装置】 同学们对甲组左盘中的反应装置进行了如下三种改进,你认为最佳装置是(填序号)___,从另外两种装置中任选一种指出其不足:________。
【得出结论】 同学们利用改进后的最佳装置进行再次探究,均得出猜想2正确。进一步
分析发现,反应体系中器材和未参加反应的物质的质量在反应前后保持不变,最终得出结论:_________________________的各物质的质量总和等于反应后生成的各物质的质量总和。
【解释应用】
解释:化学反应前后,原子的种类、数目、质量均不变,所以质量守恒。
应用:某固体物质受热会发生分解反应,生成氧化铜、水和二氧化碳三种物质,则该固体物质一定由_________种元素组成。