题目内容
若金属锰(Mn)在金属活动性顺序中位于铝和锌之间,则下列反应不正确的是
A.Mn + H2SO4 = MnSO4 + H2↑ B.Mg + MnSO4 = MgSO4 + Mn
C.Fe + MnSO4 = FeSO4 + Mn D.Mn + CuSO4 = MnSO4 + Cu
【答案】
C
【解析】A、锰在氢的前面,能与酸发生置换反应生成氢气,故能反应;
B、锰位于铝和锌之间,说明在镁的后面,能被镁从其盐溶液中置换出来,故能反应.
C、锰位于铝和锌之间,说明在铁的前面,铁不能与硫酸锰发生置换反应,故不能反应;
D、锰在铜的前面,能与硫酸铜发生置换反应,故能反应;,
故选C.

练习册系列答案
相关题目
人类的生产生活离不开金属,
(1)下列三种金属被发现、使用的先后顺序依次为:铜、铁、铝.金属大规模被使用的先后顺序跟______(填序号)选项关系最大.
①地壳中金属元素的含量;②金属的导电性;③金属的活动性.
(2)北京奥运会用到多种材料.下列应用中使用金属材料的有______ (填序号).
①使用金、银和铜等制作奖牌 ②使用纯羊毛和聚酯纤维制作“福娃,,
③使用新型钢材建造“鸟巢”④使用聚氟乙烯制造“水立方”外层膜
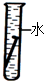
(3)现在世界上每年因腐蚀而报废的金属设备和材料相当于年产量的20%-40%.下列各种情况铁钉最易生锈的是______.
A、 B、
B、 C、
C、 D、
D、
(4)为探究锰与铁的金属活动性,在相同温度下,取大小相同、表面光亮的两种金属薄片,分别投入等体积、等溶质质量分数的足量稀盐酸中(反应中Mn显+2价),请回答:
| 金属 | 铁 | 锰 |
| 与盐酸反应现象 | 放出气泡速率缓慢 | 放出气泡速率较快 |
| 结论 | 活动性铁______(填“>”“<”)锰 | |
(5)将盛有等质量、等溶质质量分数的稀盐酸的两只烧杯,放在托盘天平左右两盘上,调节至平衡,再向两只烧杯中分别放入质量相等的镁和铁,待反应停止后,请判断:
①若天平仍保持平衡,烧杯中一定没有剩余的物质是______;
②若天平失去平衡,则指针一定偏向放______的一边.
人类的生产生活离不开金属,
(1)下列三种金属被发现、使用的先后顺序依次为:铜、铁、铝.金属大规模被使用的先后顺序跟 (填序号)选项关系最大.
①地壳中金属元素的含量;②金属的导电性;③金属的活动性.
(2)北京奥运会用到多种材料.下列应用中使用金属材料的有 (填序号).
①使用金、银和铜等制作奖牌 ②使用纯羊毛和聚酯纤维制作“福娃,,
③使用新型钢材建造“鸟巢”④使用聚氟乙烯制造“水立方”外层膜
(3)现在世界上每年因腐蚀而报废的金属设备和材料相当于年产量的20%-40%.下列各种情况铁钉最易生锈的是 .
A、 B、
B、 C、
C、 D、
D、
(4)为探究锰与铁的金属活动性,在相同温度下,取大小相同、表面光亮的两种金属薄片,分别投入等体积、等溶质质量分数的足量稀盐酸中(反应中Mn显+2价),请回答:
除了比较与酸反应产生气体速率的快慢,请你再举出一种可比较这二种金属活动性强弱的方法(写出所需药品即可): .
(5)将盛有等质量、等溶质质量分数的稀盐酸的两只烧杯,放在托盘天平左右两盘上,调节至平衡,再向两只烧杯中分别放入质量相等的镁和铁,待反应停止后,请判断:
①若天平仍保持平衡,烧杯中一定没有剩余的物质是 ;
②若天平失去平衡,则指针一定偏向放 的一边.
(1)下列三种金属被发现、使用的先后顺序依次为:铜、铁、铝.金属大规模被使用的先后顺序跟 (填序号)选项关系最大.
①地壳中金属元素的含量;②金属的导电性;③金属的活动性.
(2)北京奥运会用到多种材料.下列应用中使用金属材料的有 (填序号).
①使用金、银和铜等制作奖牌 ②使用纯羊毛和聚酯纤维制作“福娃,,
③使用新型钢材建造“鸟巢”④使用聚氟乙烯制造“水立方”外层膜
(3)现在世界上每年因腐蚀而报废的金属设备和材料相当于年产量的20%-40%.下列各种情况铁钉最易生锈的是 .
A、
 B、
B、 C、
C、 D、
D、
(4)为探究锰与铁的金属活动性,在相同温度下,取大小相同、表面光亮的两种金属薄片,分别投入等体积、等溶质质量分数的足量稀盐酸中(反应中Mn显+2价),请回答:
| 金属 | 铁 | 锰 |
| 与盐酸反应现象 | 放出气泡速率缓慢 | 放出气泡速率较快 |
| 结论 | 活动性铁 (填“>”“<”)锰 | |
(5)将盛有等质量、等溶质质量分数的稀盐酸的两只烧杯,放在托盘天平左右两盘上,调节至平衡,再向两只烧杯中分别放入质量相等的镁和铁,待反应停止后,请判断:
①若天平仍保持平衡,烧杯中一定没有剩余的物质是 ;
②若天平失去平衡,则指针一定偏向放 的一边.
 B、
B、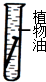 C、
C、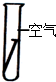 D、
D、