题目内容
(2009?抚顺)在实验室里,同学们找到了烧碱溶液、氯化钡溶液、稀硫酸、水四种试剂进行实验.
(1)将上述四种试剂两两混合,能生成白色沉淀的两种试剂是
(2)从上述四种试剂中选择合适的试剂.除去下列物质中的少量杂质的少量杂质(括号内为杂质).把选择的试剂填写在相应的横线上.
CaCO3粉末(Na2CO3)
(1)将上述四种试剂两两混合,能生成白色沉淀的两种试剂是
氯化钡溶液和稀硫酸(或BaCl2和H2SO4)
氯化钡溶液和稀硫酸(或BaCl2和H2SO4)
;能产生反应但无明显现象的两种试剂是烧碱溶液和稀硫酸(或NaOH和H2SO4)
烧碱溶液和稀硫酸(或NaOH和H2SO4)
.(2)从上述四种试剂中选择合适的试剂.除去下列物质中的少量杂质的少量杂质(括号内为杂质).把选择的试剂填写在相应的横线上.
CaCO3粉末(Na2CO3)
水(或H2O)
水(或H2O)
;H2(CO2)烧碱溶液(或氢氧化钠溶液或NaOH)
烧碱溶液(或氢氧化钠溶液或NaOH)
.分析:本题中给出四种试剂,让其两两反应,氯化钡溶液和稀硫酸反应会生成硫酸钡白色沉淀和盐酸.酸和碱反应会生成盐和水,无明显现象.一般的除杂质题必须同时满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应②反应时不能加入新的杂质.CaCO3粉末中混有Na2CO3,碳酸钙不溶于水,可以用水除去;杂质二氧化碳可以考虑用碱溶液吸收.
解答:解:(1)氯化钡溶液和稀硫酸反应会生成硫酸钡白色沉淀和盐酸;烧碱溶液和稀硫酸反应,生成硫酸钠和水,无明显现象.故答案为:氯化钡溶液和稀硫酸(或BaCl2和H2SO4);烧碱溶液和稀硫酸(或NaOH和H2SO4)
(2)CaCO3粉末中混有Na2CO3,碳酸钙不溶于水,碳酸钠易溶于水,可以用水除去;杂质二氧化碳可以考虑用烧碱溶液吸收,因为氢气与烧碱不反应.故答案为:水(或H2O);烧碱溶液(或氢氧化钠溶液或NaOH)
(2)CaCO3粉末中混有Na2CO3,碳酸钙不溶于水,碳酸钠易溶于水,可以用水除去;杂质二氧化碳可以考虑用烧碱溶液吸收,因为氢气与烧碱不反应.故答案为:水(或H2O);烧碱溶液(或氢氧化钠溶液或NaOH)
点评:本考点既考查了酸碱盐的性质,又考查了物质的分离或净化的探究,是中考的重点也是一个难点,要加强记忆除去常用离子的方法,根据酸碱盐反应的条件、物质的溶解性和除杂质的条件,要认真分析,综合把握.本考点经常出现在选择题、填空题和实验题中.

练习册系列答案
相关题目
 (2009?抚顺)(1)请将右图所示物质按要求填写在横线上.
(2009?抚顺)(1)请将右图所示物质按要求填写在横线上.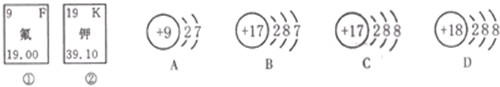
 (2009?抚顺)右图中a、b、c是三种固体物质的溶解度曲线.
(2009?抚顺)右图中a、b、c是三种固体物质的溶解度曲线.