题目内容
【题目】如图1为溴原子(Br)的结构示意图;如图2为A、B、C、D、E5种粒子的结构示意图.请回答下列问题:
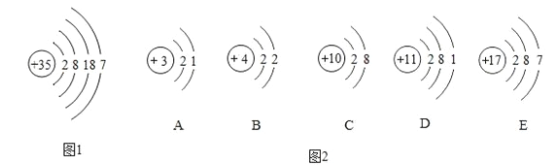
(1)图1中第三层电子数与最外层电子数之差为______(注意:不能填代数式);图2中E粒子形成的单质的化学式是_______(填用元素符号表示的化学式).
(2)D粒子与溴原子可以结合成化合物,该化合物的化学式为______(填用元素符号表示的化学式).
(3)图2的结构示意图中,_______(填字母代号)表示的是非金属元素的粒子.
【答案】 9 Cl2 NaBr E
【解析】A、由图可知,第三层的电子数为18,最外层的电子数为7,故差为11;图2中E粒子是氯原子,它形成的单质是双原子单质,化学式为Cl2;(2)D粒子是钠原子,形成化合物时显+1价,溴原子的最外层电子数为1,形成化合物时显-1价,故化学式为NaBr;(3)原子结构示意图中最外层电子数大于等于4时为非金属元素,故选E。

练习册系列答案
相关题目